蓝藻菌素中含有高度官能化的 γ-丁内酯核心,γ-丁内酯是指 1,4 位羟基和羧基自缩合形成一个内酯环的化合物,这种结构特征广泛存在于其他来源不同的呋喃内酯天然产物家族中,但呋喃内酯在 γ-丁内酯的前提下还必须在 4 位(γ)碳存在一个双键,这样的结构因为双键的伸缩振动具有类似呋喃环的芳香性质。可以说,蓝藻菌素既是一种呋喃内酯,也是一种 γ-丁内酯。

▲图丨各成分结构图
光系统 II(或水 - 质体醌氧化还原酶 )是氧光合作用的光依赖性反应中的第一个蛋白质复合物。它位于植物、藻类和蓝细菌的类囊体膜中。在光系统中,酶捕获光的光子以激发电子,然后通过各种辅酶和辅因子转移电子以将质体醌还原为质体酚。电子氧化水而被取代,形成氢离子和分子氧。通过光解水得到的电子来补充丢失的电子,光系统 II为所有光合作用提供电子。
近日,来自德累斯顿工业大学的 Tobias Gulder 教授和来自莱比锡大学的 Tanja Gulder 教授团队通过研究首次阐明了蓝藻菌素的生物合成途径,并在研究过程中意外发现了一种新的呋喃内酯合成酶,或可作为一种催化工具用于该类化合物的生物合成,研究成果以“Biosynthesis of cyanobacterin, a paradigm for furanolide core structure assembly”为题发表在nature chemical biology上。

(来源:nature chemical biology)
首次阐明蓝藻菌素的生物合成路径
呋喃内酯天然产物家族包括来自蓝藻地衣共生体的细胞毒性结节素 I、来自黏菌的抗生素增强素和血管内酯等。但几十年来,即使随着生物信息学等工具的发展,组装蓝藻菌素和具有 γ-丁内酯相关结构的呋喃内酯天然产物的酶机制也未能确定,这表明呋喃内酯的组装涉及不寻常的生物合成逻辑。

▲图丨若干具有γ-丁内酯核心结构的成分(来源:研究论文)
呋喃内酯核心结构的组装模式或表明它是由三种氨基酸前体组装而成。这需要通过三个氨基酸前体在 C-alpha 位置进行缩合反应,但只靠 C-alpha 位置进行缩合反应无法形成 C-C 键,呋喃内酯核心结构也无法形成。因此需要一种新的酶促策略,通过进行相容的 C-alpha 反应来实现三个氨基酸构建块的融合。
Tobias Gulder 联手 Tanja Gulder 的研究团队通过结合生物信息学、合成生物学、酶学和生物化学分析等多种现代工具
探索如何产生呋喃内酯的碳骨架中的核心部分,并试图阐明呋喃内酯生物合成的目标发现和表征的蓝藻菌素(cyb)生物合成基因簇(BGC)编码,最终发现了呋喃内酯生物合成的一般范式和 C-C 键形成的生物化学规律。
首先,该团队从含有卤素酶结构域出发,发现了蓝藻中呋喃内酯类生物合成基因簇(cyb-BGC),并用“直接通路克隆”(DiPaC)的方法克隆了蓝藻中呋喃内酯类生物合成基因簇(cyb-BGC)。DiPaC 是一种新的合成生物学方法,由 Tobias Gulder 实验室开发,可快速有效地将整个天然产物的生物合成途径转入重组宿主系统。
接下来,研究小组以大肠杆菌为细胞工厂,在其中表达所有关键酶,通过分离并研究每个酶的功能,得出了蓝藻细菌生物合成蓝藻菌素的基本步骤。令研究人员惊喜的是,他们遇到了一类以前没被发现的呋喃内酯合成酶,并通过同位素标记、基因敲除以及化学和遗传互补实验等方法提供的呋喃内酯生物合成的早期步骤的决定性画面,确定了蓝藻菌素核心结构组装所需的四种酶 cybC、cybF、cybE 和cybB,这四种酶组成了呋喃内酯合成酶的最小合成单元。
其中 cybE 利用酪氨酸与缬氨酸合成一种含有苯环的酮酸, cybB 和 cybC 利用一分子香豆酸和酪氨酸合成另一种酮酸,再利用 cybF 分子催化,通过 C-C 键构建在一起,从而形成呋喃内酯结构框架。在对这些呋喃内酯合成酶的进一步研究中,这些酶被证明是高效的体外生物催化剂。

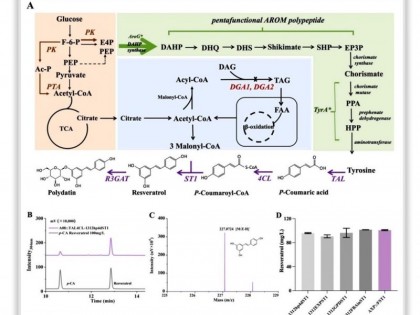
▲图丨呋喃内酯核心结构的生物合成机理(来源:研究论文)
“计划寻找更多的新型催化剂”
Tanja Gulder 教授表示,“有了呋喃内酯合成酶,我们可以获得一种酶的工具,它将使我们能够在未来开发更环保的方法来生产生物活性化合物,从而为更可持续的化学做出重大贡献。接下来,我们计划在其他生物中寻找这些新型的生物催化剂,从而在天然产物类别中找到新的生物活性成员,并开发蓝藻菌素的生物技术生产和结构多样化的方法。”
天然产物是自然界长期进化的物质实体,是生物活性物质和实用药物发现的重要源泉。这些具有特殊生物活性的次生代谢物大多结构新颖,活性显著,一直以来作为发现重要先导化合物的源泉而颇受关注。深入了解大自然如何合成组装这些化合物,对基于此类化合物的药物的开发和生产至关重要。
此次,两所大学的研究团队扩展了 γ-丁内酯形成的生物合成和生物催化工具箱,具有较大指导意义。有业内人士表明,该研究工作全面详细地解析了 γ-丁内酯结构骨架分子的生物合成过程与化学反应机理,以及 γ-丁内酯碳骨架组成过程中的底物选择性问题,
为呋喃内酯类化合物的基因工程奠定了理论与设计基础。
“但该工作也有不足,其一,虽全面解析了呋喃内酯骨架的生物合成过程,通过缺失回补实验发现了最小合成单元,但蓝藻中呋喃内酯类生物合成基因簇(BGC)中其
他蛋白的功能均未进一步研究
,其中的卤素酶是否直接参与蓝藻菌素的生物合成仍然未知;
其二,
呋喃内酯类化合物对蓝藻自身的生长与发育影响并未提及,呋喃内酯类化合物缺失或不同组成的突变体是否表现出不同的生理特性也未提及;
其三,
没有进一步结合酶的蛋白质结构进行催化机理的解析,电子转移等层面的问题也无从得知。
”
不可否认的是,该研究首次阐明自然产物蓝藻菌素的生物合成途径,为呋喃内酯的生物合成提供了一个通用的范式,也为全面开发用于医学和农业的天然产物铺平了道路。