浙大团队调控改造酿酒酵母生成虾青素产量高达446.4mg/L


日期:2022-08-29
来源:生辉SynBio 浏览:
2130 评论:0 核心提示:自 2013 年,叶丽丹所在的课题组就开始通过代谢改造微生物来合成虾青素,与大肠杆菌相比,酿酒酵母是公认安全(GRAS)的底盘系统,具有更广阔的应用场景,且不存在噬菌体污染的风险,因此该团队选择以酿酒酵母为细胞工厂来合成虾青素。前期该团队已经开发了方便酿酒酵母遗传操作的工具并构建了可控的 β-胡萝卜素生物合成途径,在此基础上进行途径延伸即可获得产虾青素酿酒酵母菌株。“但在这过程中遇到了两个问题:一是催化 β-胡萝卜素转化生成虾青素的 β-胡萝卜素酮化酶和 β-胡萝卜素羟化酶活性较低,形成限速步骤并造成中间
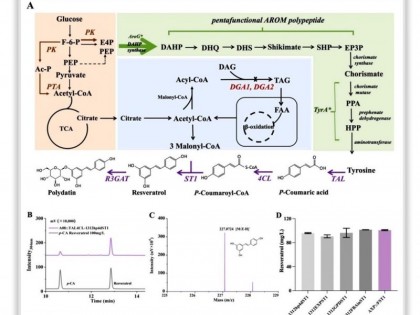
自然界中有一种色素,它存在于大多数甲壳类动物、鲑科鱼类、鸟类的羽毛和肉冠,使这些动物呈现出红色。这种色素被称作“虾青素”。虾青素,又名虾黄质、龙虾壳色素,是一种类胡萝卜素,也是类胡萝卜素合成的最高级别产物。1938 年,德国化学家理查德·库恩(Richard Kuhn)最早从龙虾体内提取并鉴定出这种色素。在活体虾中,虾青素与蛋白质结合,光学特性发生改变而呈现出蓝色,加热之后,蛋白质变性释放出虾青素并显示出红色。虾青素也被公认为第 4 代抗氧化素,是迄今人类发现的最强抗氧化单分子物质。据悉,其抗氧化活性是维生素 E 的 1000 倍、葡萄籽的 17 倍、番茄红素的 20 倍、硫辛酸的 75 倍。目前虾青素的生产方法主要为化学法和生物提取法,不过这两种方式各有弊端。近年来,随着合成生物技术的发展,构建微生物细胞工厂合成虾青素已成为可能。近日,浙江大学化学工程与生物工程学院副教授叶丽丹课题组在 ACS Synthetic Biology 发表了以“Spatiotemporal Regulation of Astaxanthin Synthesis in S. cerevisiae”为题的文章,通过结合空间调控和时间调控,最终产生了 446.4mg/L 的虾青素。指的是时间和空间两个维度的调控,实质上是通过合理控制虾青素合成的时机以及适度扩展虾青素的胞内储存空间来提高酿酒酵母的虾青素产量。这是因为虾青素的合成与酵母细胞自身的生长代谢争夺胞内资源,并且虾青素作为亲脂性产物,其疏水特性与细胞内部的亲水环境之间的矛盾导致虾青素主要储存在酵母细胞的膜结构中,影响了细胞膜的流动性,对细胞的正常生理活动造成不良影响,同时这一特性也造成了储存空间有限的问题,最终限制了虾青素的产量。
叶丽丹于 2000-2004 年和 2004-2006 年分别在浙江大学生命科学学院获得理学学士和硕士学位,2006-2010 年通过德国耶拿大学、莱布尼茨天然产物研究与感染生物学研究所和马普化学生态研究所合办的博士生项目获得理学博士学位。2010-2013 年在新加坡国立大学和新加坡科技研究局从事工业生物技术方面的博士后研究,具体研究方向为通过木质纤维素原料的生物转化合成乳酸和乙醇等大宗化学品。正式接触合成生物学是 2013 年 8 月回国加入浙江大学化学工程与生物工程学院于洪巍教授课题组之后。她现为浙江大学化学工程与生物工程学院副教授、博士生导师,研究方向为微生物代谢工程、蛋白质工程和合成生物学。
目前酿酒酵母改造菌株报道的最高产量,但离工业化仍有距离叶丽丹表示,化学合成的虾青素为三种构型的混合物即 25% (3S-3'S),25%(3R-3'R)和 50%(3R-3'S),生物吸收效果差,生物学活性不高,且可能引入化学杂质。她补充道,生物提取的来源包括虾壳废弃物、红法夫酵母和雨生红球藻。由于虾壳废弃物成分复杂,虾青素的含量相对低,目前很难大规模地从水产品废弃物中提取虾青素。红法夫酵母和雨生红球藻为虾青素的天然生产者,但红法夫酵母生产的虾青素为生理活性较低的(3R-3'R)构型,且对于培养基要求较高、发酵温度较低,限制了其大规模的工业化应用。雨生红球藻是目前天然虾青素的主要来源,且为高生物活性的左旋(3S-3’S)形式,但由于雨生红球藻培养过程需要长时间的光照以及大量的淡水培养,且下游分离难度大,生产成本较高。自 2013 年,叶丽丹所在的课题组就开始通过代谢改造微生物来合成虾青素,与大肠杆菌相比,酿酒酵母是公认安全(GRAS)的底盘系统,具有更广阔的应用场景,且不存在噬菌体污染的风险,因此该团队选择以酿酒酵母为细胞工厂来合成虾青素。前期该团队已经开发了方便酿酒酵母遗传操作的工具并构建了可控的 β-胡萝卜素生物合成途径,在此基础上进行途径延伸即可获得产虾青素酿酒酵母菌株。“但在这过程中遇到了两个问题:一是催化 β-胡萝卜素转化生成虾青素的 β-胡萝卜素酮化酶和 β-胡萝卜素羟化酶活性较低,形成限速步骤并造成中间产物积累,为此我们通过蛋白质的体内定向进化来提高这两个限速酶的活性并通过调整这两个限速酶的基因拷贝数来减少中间产物积累。”二是虾青素异源合成对酿酒酵母底盘细胞造成压力,生物量和产率难以兼顾,为此我们建立了温度响应型的动态代谢调控策略和基于多功能基因组编辑的脂滴调控策略,通过调控虾青素的合成时机和储存空间来缓解生长与生产之间的矛盾,提高虾青素的产量。”在上述文章中,叶丽丹团队通过前期开发的温度响应型动态代谢调控策略在培养过程中通过改变温度来适时启动虾青素生物合成途径基因的表达,使细胞生长和虾青素合成分阶段进行,从而减少两者之间的相互干扰,并通过对脂质合成和脂滴形态相关基因的综合调控实现脂滴数量和大小的适度增加,为虾青素提供更多的胞内疏水性储存空间。不过叶丽丹也坦言,此虾青素产量虽是目前酿酒酵母改造菌株中报道的最高产量,但是离工业化生产还有一定的距离。前期他们的工作主要集中于菌株的代谢改造,在发酵条件方面没有进行深入的探究,之后将在进一步途径改造的基础上优化发酵工艺,提高产量。除了虾青素,叶丽丹团队还通过构建与调控微生物细胞工厂实现了辅酶 Q10(抗氧化剂)、生育三烯酚(维生素 E 重要成分)、视黄醇(维 A 醇)、视黄酸(维 A 酸)、7-脱氢胆固醇(维生素 D3 前体)、叶黄素(视网膜黄斑组分)、斑蝥黄(饲料添加剂)、香紫苏醇(香精香料)、异戊二烯(异戊橡胶单体)、ω-氨基月桂酸(尼龙 12 单体)等一系列功能化学品和材料单体的生物合成。其中辅酶 Q10 已经实现工业化生产,生育三烯酚、视黄醇、虾青素等几个产品正在推进中。同时,该团队还通过蛋白质工程手段获得了催化性能改善的短链脱氢酶、酯酶、醛缩酶等,实现了一系列手性药物前体的生物催化法合成并实现了工业化生产。以生育三烯酚为例,它是维生素 E 的重要成分。维生素 E 是维持机体正常代谢和机能的必需维生素,包含 α、β、γ、δ-生育酚(Tocopherol)和 α、β、γ、δ-生育三烯酚(Tocoterienol)共 8 种化合物。由于生育三烯酚含有不饱和侧链,能更有效地渗透于含有饱和脂肪酸层的组织中,也能更好地分布在细胞膜脂质层内。因此相比于生育酚,生育三烯酚具有更强的抗氧化和清除自由基的功能,并且在抑制胆固醇、关节支持以及心血管健康问题等方面有着显著优势,是食品、医药等行业潜在的功能性原料。目前国外已有相应膳食补充剂上市,功效成分主要为植物提取的 4 种天然生育三烯酚。目前 DL-α-生育酚的化学合成非常成熟,且成本低廉,但生育三烯酚尚未实现商业化的化学合成,并且在植物中的分布相对较少,限制了其进一步的开发和应用。2020 年,叶丽丹所在的团队就在 Nature Communications 上发表以“Fermentative production of Vitamin E tocotrienols in Saccharomyces cerevisiae under cold-shock-triggered temperature control”为题的文章,通过将来自光合生物的异源基因与内源性莽草酸途径和甲羟戊酸途径相结合,运用冷激触发温控系统,使生育三烯酚滴度达 320mg/L。这项工作为发酵生产维生素 E 打下了坚实的基础,而开发的低温触发控制系统也为酵母中天然产物的生物合成提供了强大的调节工具。采访最后,叶丽丹也对合成生物学在生产天然产物中发挥的作用发表了自己的看法,她认为一些重要的天然产物结构复杂且具有多个手性中心,造成化学合成工艺过于复杂难以实现工业化,而从植物等天然生产者中提取则往往受限于含量低、生长周期长、占用土地资源、受气候影响大等问题。通过合成生物学方法进行途径重构和合理调控从而实现天然产物的高效生物制造,具有绿色、环保、占地少、生产周期短等优点,发展前景广阔。