硝化是合成用于药品、农药和炸药的硝基化合物的一个主要过程。工业上生产硝基化合物不仅反应条件苛刻,还伴随着区域选择性差、环境污染严重等问题。
对比之下,生物催化硝化则反应条件温和,且对环境友好。然而,这种看似很有前途的硝基化合物制备方法却一直开发较少,最大的问题在于缺乏原生的硝化酶和/或酶的底物范围狭窄。
例如,N-加氧酶(N-oxygenase)只能将氨基官能团转化为硝基官能团;在细菌、真菌、植物和动物中发现的许多过氧化物酶可以有效地催化芳香族化合物的直接硝化,但底物仅限于酚类和芳香族胺类。
为了满足工业应用的需求,以及为传统方法提供一个可持续的替代方案,开发新型生物硝化酶势在必行。
近日,中国科学院青岛生物能源与过程研究所(简称青岛能源所)丛志奇研究员课题组开发出用于不饱和烃直接硝化的新型工程化细胞色素 P450BM3 酶。该研究于 1 月 20 日发表在 Angewandte Chemie International Edition 上,题为“Engineering Cytochrome P450BM3 Enzymes for Direct Nitration of Unsaturated Hydrocarbons”。研究得到了山东省自然科学基金、国家自然科学基金和国家重点研发计划的支持。

(来源:Angewandte Chemie International Edition)
据了解,这是首次通过 P450 变体使用亚硝酸盐作为硝化剂使芳族直接硝化。
丛志奇表示,这项研究不仅为生物催化硝化开辟了一条新途径,也为在合成化学和合成生物学领域提升 P450 酶的过氧化物酶功能提供了新思路。
自然界已知的硝化酶仅有 N-加氧酶、过氧化物酶和细胞色素 P450 酶,且普遍存在催化效率低、底物谱窄和产物区域选择性差等不足。
在青岛能源所近年研究的基础上,丛志奇等人“乘胜追击”,锁定了 P450 酶的过氧化物酶。
据了解,青岛能源所单碳酶催化研究组在国际上首次提出双功能小分子(DFSM,N-(ω-imidazol-1-yl hexanoyl)-L-phenylalanine,Im-C6-Phe)协同 P450 酶催化概念,成功构建了人工 P450 过加氧酶催化体系;另外,研究人员利用酶化学机制指导的蛋白质工程策略,成功开发出双功能分子协同 P450 催化的过氧化物酶新功能。
与 P450 酶的单加氧酶和过氧酶活性相比,其过氧化物酶活性此前并没有受到太多的关注。在这项研究中,研究人员提出一种蛋白质工程策略,以增加细胞色素 P450BM3 过氧化物酶活性,在双功能小分子 (DFSM) 存在的情况下,直接硝化芳香族化合物和末端芳基取代的烯烃。

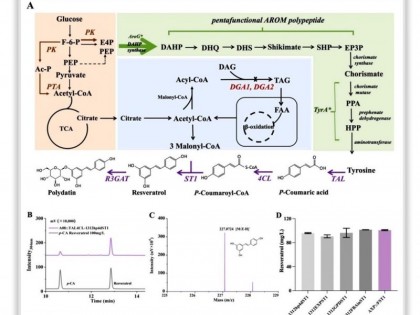
▲图丨图形概要(来源:Angewandte Chemie International Edition)
文章中指出,研究人员采用活性位点关键残基的定点突变来调节空间效应并限制底物进入,阻断了 “H-abstract and OH-rebound”的一般羟基化途径。具体来说,就是阻止底物靠近活性中心发生过加氧反应,强化其过氧化物酶功能。
另外一个令他们惊喜的结果是,大的残基也减少了底物袋的体积,从而降低了自耦合的概率。
基于此开发出工程 P450BM3 酶,几种苯酚和苯胺化合物被硝化以生成具有中等至高总周转数的邻硝化和对硝化产物。
之后他们进一步扩大底物范围,证明了 DFSM 促进的 P450 过氧化物酶系统可用于苯乙烯及其衍生物的乙烯基的硝化。在此之前,烯烃的直接酶硝化没有被报道过。
根据资料,此研究开发的工程酶底物谱范围覆盖 19 个芳香化合物和 9 个末端芳基烯烃化合物,是迄今为止催化效率最高、底物范围最广的人工 P450 硝化酶。
这项研究为开发硝化 P450 酶提供了新的见解,并且已经通过晶体学研究和自由基控制实验得到了进一步的支持。
在文章最后,作者表示,目前实验室正在进一步研究,以提高这种 DFSM 促进的 P450 酶硝化系统的催化效率、区域选择性和底物杂交性。