程功, 徐建中, 张伟国 江南大学生物工程学院 工业生物技术教育部重点实验室 江苏 无锡 214122
收稿日期: 2015-07-19; 接受日期: 2015-09-23; 优先数字出版日期(www.cnki.net): 2016-06-25
基金项目: 国家高技术研究发展计划项目(863 计划) (No. 2008AA02Z212) *
通讯作者: Tel:86-510-85329312;E-mail:zhangwg168@126.com.
摘要: L-精氨酸是人体半必需的氨基酸,在生命代谢过程中起着非常重要的作用,且具有广泛的应用价值及市场需求。目前,L-精氨酸主要采用微生物发酵法进行生产,为了提高L-精氨酸的产量和稳定性,最有效的方法是优化L-精氨酸生产菌株,通过代谢工程改造微生物菌株有望达到这一目的。本文分析了微生物中L-精氨酸的代谢途径和调控机制,并综述了构建高产L-精氨酸的代谢工程策略。此外,展望了菌株稳定性和底物扩展利用的未来研究方向。
收稿日期: 2015-07-19; 接受日期: 2015-09-23; 优先数字出版日期(www.cnki.net): 2016-06-25
基金项目: 国家高技术研究发展计划项目(863 计划) (No. 2008AA02Z212) *
通讯作者: Tel:86-510-85329312;E-mail:zhangwg168@126.com.
摘要: L-精氨酸是人体半必需的氨基酸,在生命代谢过程中起着非常重要的作用,且具有广泛的应用价值及市场需求。目前,L-精氨酸主要采用微生物发酵法进行生产,为了提高L-精氨酸的产量和稳定性,最有效的方法是优化L-精氨酸生产菌株,通过代谢工程改造微生物菌株有望达到这一目的。本文分析了微生物中L-精氨酸的代谢途径和调控机制,并综述了构建高产L-精氨酸的代谢工程策略。此外,展望了菌株稳定性和底物扩展利用的未来研究方向。
关键词: L-精氨酸 代谢工程 生物合成途径 调控机制
Progress in biosynthesis and metabolic engineering of L-Arginine producer
CHENG Gong, XU Jian-Zhong, ZHANG Wei-Guo Key Laboratory of Industrial Biotechnology, Ministry of Education, School of Biotechnology, Jiangnan University, Wuxi, Jiangsu 214122, China Foundation item: National High-Tech R&D Program of China (863 Program) (No. 2008AA02Z212) *Corresponding author: Tel:86-510-85329312;E-mail:zhangwg168@126.com. Abstract: L-Arginine, a semi-essential amino acid, plays an important role in the metabolism of human life. It has a wide and expanding application in industry with a fast growing market demand. Currently, the main method of production of L-Arginine is microbial fermentation. To develop microbial strains with high productivity and stability, the most effective method is to optimize the L-Arginine producing strains. And fortunately, metabolic engineering method can be used to screen the efficient L-Arginine producing strains, and has obtained the certain success. In this mini-review, the metabolic pathway and regulatory mechanism of L-Arginine biosynthesis in microorganisms were analyzed, and the strategies for metabolic engineering the efficient L-Arginine producing strains were summarized.Furthermore, the prospects of future research about the stability of L-Arginine engineering strains and the expansions of substrate utilization were discussed.
Key words: L-Arginine metabolic engineering Biosynthetic pathway Regulatory mechanism
氨基酸是重要的生物工业材料,尤其L-精氨酸作为具有多种功能的半必需功能性氨基酸,在食品、饲料、化妆品以及医药工业具有广泛的应用[1-3]。而且,L-精氨酸在生命代谢过程中起着非常重要的作用,在人体内参与氨解毒、激素的分泌(包括生长激素、催乳素、胰岛素、胰高血糖素等)以及免疫系统等生化反应[4-8],同时L-精氨酸可以促进肌肉的形成以及伤口的愈合[9-10]。由于其潜在的医药、食品价值以及市场需求,促进了L-精氨酸的研究步伐。
自从1958年Kinoshita等[11]报道了利用谷氨酸棒状杆菌(Corynebacterium glutamicum)发酵生产L-谷氨酸,微生物发酵法生产氨基酸促进了氨基酸工业的繁荣,同时也刺激了L-精氨酸的快速发展。但是目前L-精氨酸生产菌株基本上是传统诱变选育的营养缺陷性和结构类似物抗性菌株[12-15],由于传统诱变育种具有耗时长、工作量大以及突变后的菌株变得脆弱等缺点,L-精氨酸的产量很难进一步的提高。但是代谢工程技术的发展为这一难题提供了有效的解决方法,直接的分子操作让研究者们更有目的地去改造菌株,为提高菌株L-精氨酸的产量提供了有效的解决方法。
本文主要综述代谢工程方法构建L-精氨酸工程菌的研究进展,包括L-精氨酸的代谢途径和调控机制的分析,高产L-精氨酸工程菌株的代谢工程构建策略,并展望了菌株稳定性以及底物扩展利用的未来研究方向。
1 L-精氨酸的生物合成途径
L-精氨酸是谷氨酸家族的氨基酸,是以谷氨酸作为前体物质,共经过7−8种酶的催化最终合成L-精氨酸。在微生物体内L-精氨酸的生物合成途径有3种,如图 1所示。根据乙酰基团参与的方式L-精氨酸在微生物体内的生物合成途径可以分为3种:(1) 线性途径:主要存在于Enterobacteriaceae[16]和Myxococcus xanthus[17]体内。L-谷氨酸首先经由argA编码的N-乙酰谷氨酸合成酶(NAGS)催化合成N-乙酰谷氨酸(NAG),再经argB、argC、argD、argE、argF、argG、argH编码的各酶催化最终合成L-精氨酸。(2) 循环途径:广泛存在于酵母、藻类、植物以及大部分细菌体内,例如Bacillus stearothermophilus[18]、Saccharomyces cerevisiae[19]、Thermotoga maritime[20]、Pseudomonas aeruginosa[21]和Corynebacterium glutamicum[22]等。在循环途径中,N-乙酰谷氨酸是在N-乙酰鸟氨酸经过argJ编码的鸟氨酸乙酰转移酶催化下将乙酰基转移至L-谷氨酸上生成的,接着N-乙酰谷氨酸再经过由argB编码的N-乙酰谷氨酸激酶(NAGK)磷酸化,然后经过argC、argD、argJ、argG、argH编码的各酶催化下最终合成L-精氨酸。鸟氨酸乙酰转移酶(argJ基因编码)在不同微生物中具有单功能和双功能两种类型,单功能的鸟氨酸乙酰转移酶只具有线性途径中的乙酰鸟氨酸酶(argE基因编码)的功能,只对乙酰鸟氨酸具有脱乙酰的能力;而在此途径中双功能的鸟氨酸乙酰转移酶具有线性途径中乙酰谷氨酸合成酶(由argA基因编码)和乙酰鸟氨酸酶的双重功能,乙酰鸟氨酸在鸟氨酸乙酰转移酶作用下生成鸟氨酸,但同时,乙酰基团又被循环转移到L-谷氨酸而形成乙酰谷氨酸,从而使乙酰基团得到了循环利用,因此此途径又称为经济循环途径。(3) Shi等[23]在一种黄单胞菌(Xanthomonas campestris)中发现一种L-精氨酸合成新途径:乙酰鸟氨酸没有脱乙酰生成鸟氨酸,而由乙酰鸟氨酸氨甲酰转移酶(argF′编码)催化生成乙酰瓜氨酸,它再由乙酰瓜氨酸催化脱乙酰生成L-瓜氨酸,而后再由L-瓜氨酸合成L-精氨酸。argF′的同源基因同时发现于Xylella、Bacteriodes、Cytophaga以及其他的Eubacteria的胞内。

图 1 微生物菌体内L-精氨酸的生物合成途经
Figure 1 Biosynthetic pathway of L-Arginine in microorganisms
A: Linear biosynthetic pathway of L-arginine; B: Circulation biosynthetic pathway of L-arginine; C: New biosynthetic pathway of L-arginine. argA: Acetylglutamate synthase; argJ: Ornithine acetyltransferase; argB: Acetylglutamate kinase; argC: Acetylglutamate semialdehyde dehydrogenase; argD: Acetylornithine transaminase; argE: Acetylornithine deacetylase; argF: Ornithine transcarbamylase; argF′: Acetylornithine carbamoyltransferase; argG: Argininosuccinate synthase; argH: Arginosuccinase.
2 L-精氨酸合成相关的调控机制
微生物细胞内存在复杂的代谢网络,许多分子的合成都在DNA或蛋白质层次上受到严格调控,L-精氨酸的合成也不例外。L-精氨酸合成途径中的一些关键酶受到产物反馈抑制或阻遏作用,同时胞内的L-精氨酸的胞外分泌也受到相应调控。因此,要对L-精氨酸产生菌进行理性的代谢工程优化,必需对其调控机制进行全面了解。
2.1 L-精氨酸生物合成途径中的反馈抑制和阻遏作用
在线性途径中,L-精氨酸反馈抑制的主要对象是其合成途径的第一个酶N-乙酰谷氨酸合成酶(NAGS,由argA基因编码),其途径上催化8步反应的酶的合成都受到L-精氨酸的阻遏作用;然而在循环途径中L-精氨酸反馈抑制的主要对象是其合成途径中的第二个酶N-乙酰谷氨酸激酶(NAGK,由argB基因编码),其合成途径中各步酶的合成大部分受到L-精氨酸的阻遏作用[24]。
除了L-精氨酸对关键酶基因的反馈抑制作用,在L-精氨酸生物合成途径中还存在ArgR/AhrC+ L-精氨酸协同反馈的负控制阻遏体系,主要是由L-精氨酸作为辅阻遏物与精氨酰-tRNA阻遏蛋白ArgR/AhrC结合对精氨酸的合成途径中各个操纵子所进行的转录水平调节。参与调控L-精氨酸生物合成途径中的阻遏蛋白ArgR首先在E. coli中发现,而在Bacillus subtilis发现另一阻遏蛋白AhrC参与调控L-精氨酸的合成,但是在Lactococcus lactis中发现阻遏蛋白ArgR和AhrC同时参与L-精氨酸生物合成的调控[25-27]。Larsen等对L. lactis的阻遏蛋白ArgR和AhrC进行转录组分析发现,阻遏蛋白主要与精氨酸生物合成中的argC基因和精氨酸分解途径中arcA基因上游的启动子区域结合,从而调控argC和arcA基因的表达,进而调控L-精氨酸的合成[28]。在Pseudomonads中同样发现了L-精氨酸阻遏蛋白ArgRp,ArgRp阻遏蛋白首先在P. aeruginosa中发现[29-30]。作为aotJQMOP-argR操纵子的最后一个基因,argR基因调控着L-精氨酸和L-鸟氨酸的生物合成以及分解代谢[31]。研究发现ArgRp阻遏蛋白在Pseudomonads中同时调控L-精氨酸生物合成途径中的基因(argF,argG和carAB)以及L-谷氨酸生物合成途径中的基因(gltBD和gdhA)。ArgRp阻遏蛋白同时还是许多操纵子和基因转录的激活蛋白,例如分解代谢L-精氨酸的aot操纵子,精氨酰琥珀酸转移酶途径的aru操纵子,以及分解代谢谷氨酸脱氢酶的gdhB基因[32]。最近研究发现ArgR不仅调控L-精氨酸的代谢合成,同时L-赖氨酸的生物合成也受到L-精氨酸和ArgR的协同调控[24]。另外发现另一阻遏蛋白FarR调控C. glutamicum中L-精氨酸的生物合成,阻遏蛋白FarR通过结合到arg操纵子上argC、argB、argF、argG以及gdh基因的上游区域来下调控基因的表达[33-34] 。
2.2 L-精氨酸胞外分泌的调控
终产物向胞外分泌是微生物细胞生产目的产物的最后一步,研究发现目的产物的胞外分泌是影响氨基酸产量的另一个限制性因素。因为如果胞内积累的L-精氨酸不及时分泌到胞外,就会抑制L-精氨酸生物合成途径中关键酶的活力,并弱化编码关键酶基因的转录,同时提高了胞内的L-精氨酸被分解消耗利用的机率,从而降低L-精氨酸的合成量。LysE基因是第一个被发现编码氨基酸输出蛋白的基因,在C. glutamicum中调节L-赖氨酸的胞外分泌,同时也是调控L-精氨酸胞外分泌的重要基因[35]。但是,lysE基因的表达需lysG激活蛋白以及胞内L-精氨酸或L-赖氨酸的诱导。LysE蛋白只是lysE转运蛋白大家族中的一员。另外,Nandineni和Gowrishankar在E. coli中发现了另一个编码L-精氨酸转运蛋白的基因argO (yggA)[36],argO (yggA)同样属于lysE转运蛋白家族。但是,yggA基因的表达需要L-精氨酸的诱导,而且需要argP基因编码的LysR-type的转录调节因子的辅助诱导,同时yggA基因的表达受到赖氨酸以及全转录调控子Lrp的调控[37-38]。因此,argO转运蛋白的主要功能是维持胞内精氨酸和赖氨酸的平衡,同时可以阻止有害物质的生成,例如精氨酸的结构类似物刀豆氨酸等。
3 代谢工程菌种选育状况
3.1 诱变育种
目前L-精氨酸工业生产用菌均来自传统诱变育种,因传统诱变方法操作简单、菌株遗传稳定性高,因此传统的诱变方法仍然受到部分研究者的青睐。通过选育缺陷型菌株来切断支路代谢,使代谢流流向终产物生成的方向;或是通过选育目的产物结构类似物抗性菌株,来缓解或解除目的产物的反馈抑制或(和)反馈阻遏作用。传统诱变方法基本上以上述两种方法来选育L-精氨酸的高产菌株。但传统的育种方法存在很多不足,如正突变率低,菌体突变的方向难以掌控,可能产生一些对菌株生长代谢不利的突变表型或致死型突变。而理性设计的代谢工程育种手段,目的性强,提高育种效率,可以突破这些局限性,进一步提高目的产物的产量。
3.2 代谢工程育种
总体来看,想要获得较高产量的L-精氨酸工程菌,必需从以下几个方面进行构建:(1) 解除微生物细胞自身的代谢调控机制,例如L-精氨酸生物合成过程中的反馈抑制和反馈阻遏作用;(2) 过量表达L-精氨酸生物合成途径中的基因;(3) 积累关键前体和降低副产物的合成;(4) 降低L-精氨酸的胞内消耗和提高胞外分泌。表 1总结了近些年由代谢工程手段构建的L-精氨酸产生菌的策略,以C. glutamicum为例构建L-精氨酸高产菌的方法如图 2所示。
表 1 通过代谢工程构建的L-精氨酸产生菌
Table 1 L-Arginine producing strains by metabolic engineering techniques
菌株 Strains 分子策略 Molecular strategies 产量 Titer (g/L) 参考文献 Reference
E. coli Overexpressing fbr argA,carAB and argI genes 22.1 [16]
C. glutamicum ΔargR,overexpressing argB gene (A26V/M31V) 52.0 [22]
C. crenatum Overexpressing argB gene and site-directed mutagenesis of NAGK 45.6 [39]
C. glutamicum ΔargR,ΔfarR,pgi (A1G),Psod::tkt,tal,zwf,opcA,pgl,ΔNCgl1221,Psod::carAB,Petfu::argGH 92.5 [40]
E. coli ΔargR,ΔspeC,ΔspeF,ΔadiA, overexpressing argA,argP and argO (yggA) genes 11.6 [41]
C. crenatum Heterologous and homologous overexpressing argCJBDFRGH cluster 45.3 [42]
C. crenatum Overexpressing argJ gene 42.4 [43]
C. glutamicum Overexpressing argG,argH genes of C. glutamicum and argJ gene of Bacillus stearothermophilus 25.5 [44]
C. glutamicum Overexpressing the lysE gene 35.9 [45]

图 2 L-精氨酸合成代谢工程改造策略图
Figure 2 The strategies diagrams of metabolic engineering for L-Arginine biosynthesis
ACT-CoA: Acetyl-CoA; ACTGLT: Acetylglutamate; ACTGLT-P: Acetylglutamyl phosphate; ACTGLT-SA: Acetylglutamate semialdehyde; ACTORN: Acetylornithine; α-KG: α-ketoglutarate; ARG: L-arginine; ARGSUC: Arginosuccinate; CIT: Citric acid; CITr: L-citrulline; F1,6-P: Fructose-1,6-bisphosphate; F-1-P: Fructose-6-phosphate; F-6-P: Fructose-6-phosphate; FUM: Fumaric acid; G-3-P: Glyceraldehyde-3-phosphate; G-6-P: Glucose-6-phosphate; GLC: Glucose; GLT: L-glutamate; GLU: Glutamate; ICT: Isocitric acid; OA: Oxaloacetic acid; ORN: L-ornithine; MAL,Malic acid; PEP: Phosphoenoypyruvate; PYR: Pyruvate; SUC: Succinic acid; SUC-CoA: Succinyl-CoA.
图选项
3.2.1 解除反馈抑制和阻遏作用:L-精氨酸生物合成途径中的关键酶基因都受到L-精氨酸的反馈抑制作用,如线性途径中argA基因、循环途径中的argB基因。解除L-精氨酸对关键酶基因的反馈抑制作用是进一步提高L-精氨酸产量的有效途径。Rajagopal等[16]通过将构建的包含解除反馈抑制突变株(EE11,EE17和EE51)的argA基因以及carAB和argI基因的重组质粒导入E. coli K-12中构建工程菌,结果工程菌的L-精氨酸产率是原始菌株的3−15倍。Xu等[39]在过量表达C. crenatum SYPA5-5的关键酶基因argB的基础上,对关键酶NAGK进行定点突变构建了重组菌C. crenatum SYPACCBM3,L-精氨酸耐受性实验表明重组菌弱化了反馈抑制作用,且NAGK的酶活力提高了2.76倍,L-精氨酸的产量比C. crenatum SYPA5-5提高了41.7%,L-精氨酸的产量达到45.6 g/L。
L-精氨酸生物合成过程中的酶大部分都受到阻遏蛋白基因的调控,因此解除L-精氨酸合成中的反馈阻遏作用是优化L-精氨酸生产菌的另一有效方法,主要方法是敲除阻遏蛋白基因或者下调阻遏蛋白基因的表达。Ikeda等[22]敲除了C.glutamicum ATCC 13032中的argR基因来解除反馈阻遏作用,并导入A26V和M31V定点突变的argB基因来弱化反馈抑制作用,最终工程菌的L-精氨酸产量达到52.0 g/L。Park等[40]通过敲除C. glutamicum AR1中的argR和farR基因构建AR2菌株,分批发酵L-精氨酸的产量达到61.9 g/L。Ginesy等[41]通过敲除Escherichia coli 中的argR、speC、speF(编码鸟氨酸脱羧酶)、adiA (编码精氨酸脱羧酶)基因,并导入解除反馈抑制的argA214基因构建的重组菌的L-精氨酸产量达到11.64 g/L。
3.2.2 过量表达生物合成途径中的基因:L-精氨酸生物合成过程中的7−8个酶大部分受到反馈阻遏作用,同时关键酶还受到反馈抑制作用,解除反馈抑制和阻遏作用只是在一定程度上提高了L-精氨酸的合成量,同时还需要加强L-精氨酸合成主干道的碳流,这就需要过量表达L-精氨酸生物合成途径中的基因,或者优化启动子活性来达到这一目的。在棒状杆菌中合成L-精氨酸的argCJBDFRGH基因簇由argCJBDFR和argGH两个操纵子组成。Xu等[42]将来源于C. crenatum SYPA5-5的argCJBDFRGH基因簇(argR基因已失活)构建重组质粒pJC-9039,并分别在E. coli和C. crenatum中过量表达,重组E. coli的L-精氨酸产量和各酶活力只是稍微有所提高,但是重组C. crenatum的L-精氨酸的产量提高了24.9%。Dou等[43]将来源于C. crenatum SYPA5-5中且具有双重功能的argJ基因在C. crenatum SYPA5-5中过量表达,构建重组菌SYPA5-5pJCtac-argJ,结果鸟氨酸乙酰转移酶的活力提高了90.9%,同时L-精氨酸的产量提高了16.8%。Koloyan等[44]将来源C. glutamicum的argG和argH基因以及来源于Bacillus stearothermophilus的argJ基因分别在Br. flavum HK-19A (L-精氨酸产量为25.5 g/L)中过量表达,L-精氨酸的产量均有所提高。
3.2.3 积累关键前体和降低副产物生成:L-谷氨酸是L-精氨酸生物合成的前体物质,同时也是L-脯氨酸、L-鸟氨酸和L-瓜氨酸生物合成的前体物质,其胞内浓度决定了L-精氨酸的合成速率。因此,降低L-谷氨酸的支路消耗也可以提高L-精氨酸的产量。胞内的L-谷氨酸消耗方式主要有以下几种:(1) 通过arg操纵子上的基因编码一系列酶催化生成L-鸟氨酸、L-瓜氨酸和L-精氨酸[46];(2) 通过proB、proA和proC基因编码的谷氨酸激酶、谷氨酰磷酸还原酶和Δ1-二氢吡咯-5-羧酸还原酶催化合成L-脯氨酸[47];(3) 通过L-谷氨酸输出机制分泌到胞外。第1种可以通过解除反馈抑制作用、敲除阻遏蛋白基因解除反馈阻遏作用、过量表达arg操纵子上的基因来实现L-精氨酸产量的提高,特别是调控好argF和argG基因的表达水平,从而降低L-鸟氨酸和L-瓜氨酸的积累量;第2种可以通过敲除或者弱化pro操纵子上的基因来降低L-脯氨酸的生物合成;第3种可以失活编码L-谷氨酸输出蛋白的基因来降低L-谷氨酸分泌到胞外,如Park等[40]在C. glutamicum中敲除了编码L-谷氨酸输出蛋白的Ncgl1221基因,将发酵液中的L-谷氨酸浓度从5.0 g/L降低到几乎为零。
3.2.4 降低L-精氨酸胞内消耗和提高胞外分泌:L-精氨酸在微生物体内存在4个分解代谢途径,分别如下:(1) 精氨酸酶途径。由菌体rocABC、rocDEF操纵子以及rocG基因编码的精氨酸酶以及其他酶代谢L-精氨酸参与尿素循环[48-49];(2) 精氨酸脱亚氨基酶途径。由arcDABC操纵子编码的精氨酸脱亚氨酶及其他酶催化分解L-精氨酸,此途径的重要功能是在厌氧条件下提供ATP[50-51];(3) 精氨酸琥珀酰转移酶途径。由aruCFGDBE操纵子编码的酶催化代谢L-精氨酸,此途径是在有氧条件下分解代谢L-精氨酸/L-鸟氨酸作为碳源的首要选择[52];(4) 精氨酸转氨酶/氧化酶/脱氢酶途径。此途径由不同的L-精氨酸分解代谢途径组成,但都会在不同的条件下代谢L-精氨酸[24]。在微生物体内存在如此多的L-精氨酸分解代谢途径,因此通过基因工程的手段敲除或者弱化L-精氨酸分解代谢途径中的基因表达,从而提高L-精氨酸的积累。
氨基酸的生产包括以下三部分:(1) 微生物细胞从胞外摄取碳源和能量物质;(2) 代谢底物合成中间产物,最终转化成终产物;(3) 将目的产物分泌到胞外。前两部分经过代谢工程的方法可以明显提高碳源利用率和目的产物产量,甚至终产物的浓度可以达到极限值。然而L-精氨酸如不及时运输到胞外就会提高胞内分解代谢L-精氨酸的机率,因此提高菌体目的产物的胞外分泌能力,是进一步提高胞外终产物浓度的有效途径。Xu等[45]在C. crenatum SYPA过量表达lysE基因,结果L-精氨酸的产量比对照组提高13.6%,L-精氨酸的产量达到35.9 g/L,同时降低了L-谷氨酸的浓度。Ginesy等[41]在E. coli中分别过量表达argP和argO (yggA)基因,结果L-精氨酸的产量分别提高了2倍和3倍,而且发酵液中乙酸的浓度也明显降低。
3.2.5其他方法:胞内NADPH水平是另一个可以提高L-精氨酸产量的重要因素,因为合成1 mol的L-精氨酸需要消耗3 mol的NADPH。因此提高胞内NADPH的水平,对进一步提高L-精氨酸的产率以及维持胞内氧化还原平衡是必要的措施。Rahman等[53]通过过量表达C. crenatum中的ppnk基因(编码NAD激酶),胞内NADPH和NAD的浓度分别提高了36.8%和116%,同时L-精氨酸的产量在高溶氧条件下达到26.47 g/L,比出发菌株提高了8.97%;Park等[40]在C. glutamicum AR2的基础上下调pgi基因(编码葡萄糖-6-磷酸异构酶)的表达构建菌株AR3,结果胞内NADPH的浓度提高了20%,L-精氨酸的产量比菌株AR2提高了30%。为了降低因代谢不平衡造成的葡萄糖消耗速率和细胞生长速率下降,又在菌株AR3的基础上通过sod强启动子代替原始启动子过量表达了磷酸戊糖途径中的基因(包括opcA、pgl、tal、tkt和zwf基因),构建了菌株AR4,葡萄糖的消耗速率急剧增加,同时缩短了发酵时间(从111 h缩短至72 h)。
4 展望
4.1 提高菌株的稳定性
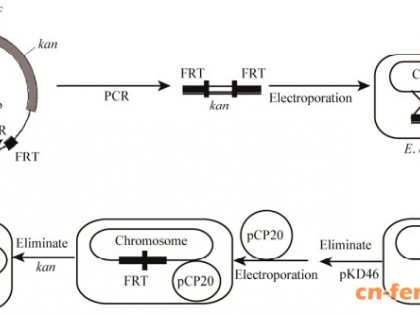
基因工程菌最大的缺点就是因为传代时重组质粒丢失而造成的遗传不稳定,从而导致工程菌发酵生产时产量不稳定,而且一些特定基因的过量表达可能造成不以利于菌株生长的因素[40-42-54]。因此含有重组质粒的工程菌在发酵过程需要添加一定浓度的抗生素提供选择压力来确保质粒的遗传稳定,同时抗生素的广泛应用容易造成抗生素污染。因此,构建的工程菌很难用于工厂生产食品和医药工业的L-精氨酸,这就迫切需要选育不带选择压力或其他类型的工程菌来保证工程菌的稳定性。常规的方法是删除染色体上非必需的基因,然后在质粒上表达同源的基因;或者敲除原始基因并导入缩短启动子的等位基因来提高导入基因的拷贝数;或者下调L-精氨酸分解代谢途径中的基因,如敲除rocF基因(编码精氨酸酶)。但是随着基因缺失和替换、启动子以及染色体技术的发展,基因可以在染色体上过表达而不用导入任何异源的遗传标记。可以通过替换强启动子来解除反馈阻遏作用,或者在染色体上替换解除反馈抑制的突变菌的等位基因来缓和反馈抑制作用[40]。所以,不带任何遗传标记的目的产物高产工程菌是目前氨基酸迫切需要的生产菌,这就为我们的研究指定了方向。
4.2 底物的扩展利用
目前氨基酸发酵工业使用的培养基成本还是普遍较高,这就为氨基酸工业可持续以及规模化发展造成了一定的压力。为降低L-精氨酸的工业发酵的成本首先就要降低发酵培养基的成本,这就需要扩展微生物菌体利用廉价的碳源,但同时不能降低目的产物的产量。生产L-精氨酸的菌株大多为棒状杆菌,棒状杆菌能够利用多种碳源,例如单糖、多糖、有机酸、以及氨基酸等,但是不能直接利用生物原料(如淀粉、纤维素、半纤维素等)。在农业和工业生产过程中总会有废料的产生,如蔗糖工业的糖蜜、农业和林业产生的小麦秸秆、玉米秸秆以及树叶等。这些生物原料都是发酵工业可开发利用的碳源,这些可再生的生物原料经过一定的简单处理可作为微生物菌体理想的碳源。本实验室利用蔗糖工业产生的废料甜菜糖蜜与葡萄糖混合碳源(质量比1:5)进行协同发酵生产L-精氨酸,L-精氨酸的产量比之前提高了5.88%。因为甜菜糖蜜中不仅含有丰富的蔗糖(47.4%),还含有丰富的微量元素(甜菜碱、氨基氮源等)。本实验室的Xu等[55]在C. glutamicum lysCfbr中异源表达fbp基因(编码果糖-1,6-二磷酸酶)和scrK基因(编码果糖激酶),将蔗糖工业废液甜菜糖蜜作为唯一碳源发酵生产L-赖氨酸,结果L-赖氨酸的产量最高提高了88.4%。另外,Park等[40]利用玉米淀粉水解液和已分解的粗糖(含有葡萄糖和果糖,来源于甘蔗)为碳源,1 500 L大规模分批发酵经代谢工程构建的工程菌C. glutamicum AR6,结果精氨酸的产量达到81.2 g/L,菌株的产能达到0.91 g/(L∙h),L-精氨酸对碳源(葡萄糖和蔗糖)的得率达到0.353 g/g。但是目前为止还未曾有微生物菌体直接利用植物秸秆、作物淀粉、纤维素等生物原材料作为碳源直接发酵生产氨基酸的报道。因此这些可再生的生物原材料的开发利用为氨基酸发酵工业提供了研究方向,并将为环保工作做出杰出贡献,大大减轻因植物秸秆焚烧造成的环境污染,对氨基酸行业的可持续发展以及环境友好型社会的建立提供了清晰的研究方向。
参考文献
[1] álvares TS, Meirelles CM, Bhambhani YN, et al. L-Arginine as a potential ergogenic aid in healthy subjects[J]. Sports Medicine, 2011, 41 (3): 233–248.
[2] Siani A, Pagano E, Iacone R, et al. Blood pressure and metabolic changes during dietary L-arginine supplementation in humans[J]. American Journal of Hypertension, 2000, 13 (5): 547–551.
[3] Böger RH. The pharmacodynamics of L-arginine[J]. Alternative Therapies in Health and Medicine, 2014, 20 (3): 48–54.
[4] Wu GY, Bazer FW, Davis TA, et al. Arginine metabolism and nutrition in growth, health and disease[J]. Amino Acids, 2009, 37 (1): 153–168.
[5] Alba-Roth J, Müller OA, Schopohl J, et al. Arginine stimulates growth-hormone secretion by suppressing endogenous somatostatin secretion[J]. The Journal of Clinical Endocrinology and metabolism, 1988, 67 (6): 1186–1189.
[6] Davis SL. Plasma levels of prolactin, growth hormone and insulin in sheep following the infusion of arginine, leucine and phenylalanine[J]. Endocrinology, 1972, 91 (2): 549–555.
[7] Thams P, Capito K. L-Arginine stimulation of glucose-induced insulin secretion through membrane depolarization and independent of nitric oxide[J]. European Journal of Endocrinology, 1999, 140 (1): 87–93.
[8] Palmer JP, Benson JW, Walter RM, et al. Arginine-stimulated acute phase of insulin and glucagon-secretion in diabetic subjects[J]. The Journal of Clinical Investigation, 1976, 58 (3): 565–570.
[9] Jobgen W, Meininger CJ, Jobgen SC, et al. Dietary L-arginine supplementation reduces white fat gain and enhances skeletal muscle and brown fat masses in diet-induced obese rats[J]. The Journal of Nutrition, 2009, 139 (2): 230–237.
[10] Barbul A, Lazarou SA, Efron DT, et al. Arginine enhances wound-healing and lymphocyte immune responses in humans[J]. Surgery, 1990, 108 (2): 331–337.
[11] Kinoshita S, Nakayama K, Akita S. Taxonomical study of glutamic acid accumulating bacteria, Micrococcus glutamicus nov[J]. Bulletin of The Agricultural Chemical Society of Japan, 1958, 22 (3): 176–185.
[12] Azuma T, Nakanishi T, Sugimoto M. Isolation and characterization of a stable L-arginine producer from continuous culture broth of Corynebacterium acetoacidophilum[J]. Journal of Fermentation Technology, 1988, 66 (3): 279–284.
[13] Utagawa T. Production of arginine by fermentation[J]. The Journal of Nutrition, 2004, 134 (10 Suppl): 2854S–2857S.
[14] Kisumi M, Takagi T, Chibata I. Construction of an L-arginine-producing mutant in Serratia marcescens: use of the wide substrate specificity of acetylornithinase[J]. The Journal of Biochemistry, 1978, 84 (4): 881–890.
[15] Cheng G, Xu JZ, Guo YF, et al. Breeding and fermentation optimization of L-arginine producing strains[J]. Microbiology China, 2016, 43 (2): 360–369. (in chinese) 程功, 徐建中, 郭燕风, 等. 常压室温等离子体诱变选育L- 精氨酸生产菌及发酵条件优化[J]. 微生物学通报, 2016, 43 (2):360–369.
[16] Rajagopal BS, DePonte J, Tuchman M, et al. Use of inducible feedback-resistant N-acetylglutamate synthetase (argA) genes for enhanced arginine biosynthesis by genetically engineered Escherichia coli K-12 strains[J]. Applied and Environmental Microbiology, 1998, 64 (5): 1805–1811.
[17] Harris BZ, Singer M. Identification and characterization of the Myxococcus xanthus argE gene[J]. Journal of Bacteriology, 1998, 180 (23): 6412–6414.
[18] Marc F, Weigel P, Legrain C, et al. An invariant threonine is involved in self-catalyzed cleavage of the precursor protein for ornithine acetyltransferase[J]. The Journal of Biological Chemistry, 2001, 276 (27): 25404–25410.
[19] Delforge J, Messenguy F, Wiame JM. The regulation of arginine biosynthesis in Saccharomyces cerevisiae[J]. European Journal of Biochemistry, 1975, 57 (1): 231–239.
[20] Fernández-Murga ML, Gil-Ortiz F, Llácer JL, et al. Arginine biosynthesis in Thermotoga maritima: characterization of the arginine-sensitive N-acetyl-L-glutamate kinase[J]. Journal of Bacteriology, 2004, 186 (18): 6142–6149.
[21] Fernández-Murga ML, Rubio V. Basis of Arginine Sensitivity of microbial N-acetyl-L-glutamate kinases: mutagenesis and protein engineering study with the Pseudomonas aeruginosa and Escherichia coli enzymes[J]. Journal of Bacteriology, 2008, 190 (8): 3018–3025.
[22] Ikeda M, Mitsuhashi S, Tanaka K, et al. Reengineering of a Corynebacterium glutamicum L-arginine and L-citrulline producer[J]. Applied and Environmental Microbiology, 2009, 75 (6): 1635–1641.
[23] Shi DS, Morizono H, Yu XL, et al. Crystal structure of N-acetylornithine transcarbamylase from Xanthomonas campestris: a novel enzyme in a new arginine biosynthetic pathway found in several eubacteria[J]. The Journal of Biological Chemistry, 2005, 280 (15): 14366–14369.
[24] Lu CD. Pathways and regulation of bacterial arginine metabolism and perspectives for obtaining arginine overproducing strains[J]. Applied Microbiology and Biotechnology, 2006, 70 (3): 261–272.
[25] Charlier D, Roovers M, Van Vliet F, et al. Arginine regulon of Escherichia coli K-12: a study of repressor-operator interactions and of in vitro binding affinities versus in vivo repression[J]. Journal of Molecular Biology, 1992, 226 (2): 367–386.
[26] Dennis CA, Glykos NM, Parsons MR, et al. The structure of AhrC, the arginine repressor/activator protein from Bacillus subtilis[J]. Acta Crystallographica. Section D, Biological Crystallography, 48 (3): 421–430.
[27] Larsen R, Buist G, Kuipers OP, et al. ArgR and AhrC are both required for regulation of arginine metabolism in Lactococcus lactis[J]. Journal of Bacteriology, 2004, 186 (4): 1147–1157.
[28] Larsen R, Kok J, Kuipers OP. Interaction between ArgR and AhrC controls regulation of arginine metabolism in Lactococcus lactis[J]. The Journal of Biological Chemistry, 2005, 280 (19): 19319–19330.
[29] Park SM, Lu CD, Abdelal AT. Cloning and characterization of argR, a gene that participates in regulation of arginine biosynthesis and catabolism in Pseudomonas aeruginosa PAO1[J]. Journal of Bacteriology, 1997, 179 (17): 5300–5308.
[30] Park SM, Lu CD, Abdelal AT. Purification and characterization of an arginine regulatory protein, ArgR, from Pseudomonas aeruginosa and its interactions with the control regions for the car, argF, and aru operons[J]. Journal of Bacteriology, 1997, 179 (17): 5309–5317.
[31] Nishijyo T, Park SM, Lu CD, et al. Molecular characterization and regulation of an operon encoding a system for transport of arginine and ornithine and the ArgR regulatory protein in Pseudomonas aeruginosa[J]. Journal of Bacteriology, 1998, 180 (21): 5559–5566.
[32] Lu CD, Yang Z, Li W. Transcriptome analysis of the ArgR regulon in Pseudomonas aeruginosa[J]. Journal of Bacteriology, 2004, 186 (12): 3855–3861.
[33] Hänßler E, Müller T, Je?berger N, et al. FarR, a putative regulator of amino acid metabolism in Corynebacterium glutamicum[J]. Applied Microbiology and Biotechnology, 2007, 76 (3): 625–632.
[34] Lee SY, Park JM, Lee JH, et al. Interaction of transcriptional repressor ArgR with transcriptional regulator FarR at the argB promoter region in Corynebacterium glutamicum[J]. Applied and Environmental Microbiology, 2011, 77 (3): 711–718.
[35] Vrljic M, Sahm H, Eggeling L. A new type of transporter with a new type of cellular function: L-lysine export from Corynebacterium glutamicum[J]. Molecular Microbiology, 1996, 22 (5): 815–826.
[36] Nandineni MR, Gowrishankar J. Evidence for an arginine exporter encoded by yggA (argO) that is regulated by the LysR-type transcriptional regulator ArgP in Escherichia coli[J]. Journal of Bacteriology, 2004, 186 (11): 3539–3546.
[37] Celis RTF. Repression and activation of arginine transport genes in Escherichia coli K12 by the ArgP protein[J]. Journal of Molecular Biology, 1999, 294 (5): 1087–1095.
[38] Peeters E, Minh PNL, Foulquié-Moreno M. Competitive activation of the Escherichia coli argO gene coding for an arginine exporter by the transcriptional regulators Lrp and ArgP[J]. Molecular Microbiology, 2009, 74 (6): 1513–1526.
[39] Xu MJ, Rao ZM, Dou WF, et al. Site-directed mutagenesis and feedback-resistant N-acetyl-Lglutamate kinase (NAGK) increase Corynebacterium crenatum L-arginine production[J]. Amino Acids, 2012, 43 (1): 255–266.
[40] Park SH, Kim HU, Kim TY, et al. metabolic engineering of Corynebacterium glutamicum for L-arginine production[J]. Nature Communications, 2014, 5 : 4618.
[41] Ginesy M, Belotserkovsky J, Enman J, et al. metabolic engineering of Escherichia coli for enhanced arginine biosynthesis[J]. Microbial Cell Factories, 2015, 14 (1): 29.
[42] Xu MJ, Rao ZM, Yang J, et al. Heterologous and homologous expression of the arginine biosynthetic argC—H cluster from Corynebacterium crenatum for improvement of L-arginine production[J]. Journal of Industrial Microbiology and Biotechnology, 2012, 39 (3): 495–502.
[43] Dou WF, Xu MJ, Cai DM, et al. Improvement of L-arginine production by overexpression of a bifunctional ornithine acetyltransferase in Corynebacterium crenatum[J]. Applied Biochemistry and Biotechnology, 2011, 165 (3/4): 845–855.
[44] Koloyan AO, Hovsepyan AS, Ghochikyan AV, et al. Construction of recombinant strains of coryneform bacteria containing homologous argG and argH Corynebacterium glutamicum genes and heterologous argJ Bacillus stearothermophilus gene[J]. Electronic Journal of Natural Sciences, 2009, 13 (2): 28–33.
[45] Xu MJ, Rao ZM, Yang J, et al. The effect of a lysE exporter overexpression on L-arginine production in Corynebacterium crenatum[J]. Current Microbiology, 2013, 67 (3): 271–278.
[46] Shin JH, Lee SY. metabolic engineering of microorganisms for the production of L-arginine and its derivatives[J]. Microbial Cell Factories, 2014, 13 (1): 166.
[47] Wan PJ, Fu KY, Lyu FG, et al. A putative Δ1-pyrroline-5-carboxylate synthetase involved in the biosynthesis of proline and arginine in Leptinotarsa decemlineata[J]. Journal of Insect Physiology, 2014, 71 : 105–113.
[48] Gardan R, Rapoport G, Débarbouillé M. expression of the rocDEF operon involved in arginine catabolism in Bacillus subtilis[J]. Journal of Molecular Biology, 249 (5): 843–856.
[49] Belitsky BR, Sonenshein AL. An enhancer element located downstream of the major glutamate dehydrogenase gene of Bacillus subtilis[J]. Proceedings of the National Academy of Sciences of the United States of America, 96 (18): 10290–10295.
[50] Barcelona-Andrés B, Marina A, Rubio V. Gene structure, organization, expression, and potential regulatory mechanisms of arginine catabolism in Enterococcus faecalis[J]. Journal of Bacteriology, 2002, 184 (22): 6289–6300.
[51] Zúñiga M, Miralles MC, Pérez-Martínez G. The product of arcR, the sixth gene of the arc operon of Lactobacillus sakei, is essential for expression of the arginine deiminase pathway[J]. Applied and Environmental Microbiology, 2002, 68 (12): 6051–6058.
[52] Itoh Y. Cloning and characterization of the aru genes encoding enzymes of the catabolic arginine succinyltransferase pathway in Pseudomonas aeruginosa[J]. Journal of Bacteriology, 1997, 179 (23): 7280–7290.
[53] Rahman MM, Qin ZQ, Dou W, et al. Over-expression of NAD kinase in Corynebacterium crenatum and its impact on L-arginine biosynthesis[J]. Tropical Journal of Pharmaceutical Research, 2012, 11 (6): 909–916.
[54] Xu JZ, Han M, Zhang JL, et al. metabolic engineering Corynebacterium glutamicum for the L-lysine production by increasing the flux into L-lysine biosynthetic pathway[J]. Amino Acids, 2014, 46 (9): 2165–2175.
[55] Xu JZ, Zhang JL, Guo YF, et al. Improvement of cell growth and L-lysine production by genetically modified Corynebacterium glutamicum during growth on molasses[J]. Journal of Industrial Microbiology and Biotechnology, 2013, 40 (12): 1423–1432.