聚酮化合物是通过聚酮合成途径产生的一大类结构和生物活性多样的次级代谢产物。链霉菌及与其亲缘关系相近的放线菌是发酵工业中聚酮类化合物的主要生产菌株[1]。聚酮化合物按照聚酮合酶(polyketide synthases,PKSs)结构以及合成机制的不同,可以分为3大类:I型聚酮,PKS是以模块形式存在的多功能酶,每一模块含有非重复使用的催化功能域,这些非重复使用的催化功能,线性化地完成聚酮合成的起始和延伸[2],例如具有抗细菌活性的红霉素(erythromycin)[3, 4]、免疫抑制活性的雷帕霉素(rapamycin)[5]、抗真菌活性的两性霉素(amphotericin)[6]、杀虫活性的阿维菌素(avermectin)[7]等均由I型PKSs合成;II型聚酮,PKS是一个多功能酶复合体,只含有一套可重复使用的独立蛋白,在聚酮合成过程中,这些蛋白被多次重复地用来催化相同的聚酮碳链缩 合反应[8],例如具有抗细菌活性的放线紫红素(actinorhodin,Act)[9]、具有抗癌活性的道诺霉素(daunorubicin,DNR)[10] 和阿霉素(doxorubicin,DXR)[11]等均由II型PKSs合成;III型聚酮,PKS与前两种PKS截然不同,它是一个同源二聚体多功能酶,聚酮合成所有催化反应均在同一个单体的活性位点完成,合成前体直接以辅酶A形式提供,不需要酰基载体蛋白(acyl carrier protein,ACP),主要负责单环和双环芳香类聚酮化合物生物合成[12, 13],例如淡黄霉素(flaviolin)[14]等均由III型PKSs合成。由于次级代谢产物不是细胞生长必须的,进化过程中,细胞产生的次级代谢产物的产量只需满足其特殊的生理功能,产量较 低[15]。但是,在工业生产时,这种低产量远不能达到产业化要求。代谢工程是目前提高次级代谢产物产量行之有效的方法。本文将从代谢工程改造实例入手,全面综述链霉菌中聚酮化合物高效生物合成的研究方法(图 1)及进展,并对利用合成生物学策略智能动态适配各个相关途径,进而提高该类化合物产量的研究思路进行展望。
 |
| 图 1. 链霉菌聚酮合成高效生产方法 Figure 1. Strategies to improve polyketide production in Streptomyces host. |
|
图选项
|
生物合成途径中的限速步骤往往反映了代谢流的控制环节,因此相应限速酶的过表达、酶活提高等都将有利于终产物合成效率的提高。其中限速酶的过表达较容易实现,是代谢工程改造中最常用的一种方法。对于聚酮合成,无论I型还是II型PKSs中的ACP都需要通过翻译后修饰连接膦酸泛酰巯基乙胺基团后才具有活性,因此负责这步反应的磷酸泛酰巯基乙胺转移酶(phosphopantetheine transferase,PPTases)是控制聚酮合成的限速酶。据报道,在I型聚酮那他霉素(natamycin,NTM)工业生产菌株Streptomyces chattanoogensis L10中存在2个PPTases (SchPPT和SchACPS)和5个PKSs (3个I型和2个II型)。其中SchPPT对5个PKSs中的ACP均可进行磷酸泛酰巯基乙胺修饰,而SchACPS仅能修饰II型PKSs中的ACP。结果在S. chattanoogensis L10中过表达SchPPT,NTM产量提高40%[16]。
虽然过表达PPTases可以达到提高聚酮化合物产量的目的,但通常仅操纵单一限速酶所达到的效果有限。代谢工程改造的实践无疑要求我们对聚酮合成途径中多个限速酶同时进行过表达。通常我们可以借助对基因簇转录谱分析确定限速酶,当然也可以通过判断发酵主产物与途径终产物之间的关系来决定哪些催化环节需要加强。例如在DXR产生菌Streptomyces peucetius ATCC 27952中糖苷配体ε-rhodomycinone与DXR的比例为20:1,明显暗示糖基合成或/与糖基转移步骤限制了DXR产量。结果在S. peucetius ATCC 27952中同时过表达相关糖基合成基因和糖基转移酶基因,DXR产量提高5.6倍[17]。
2 过表达途径特异性激活蛋白聚酮化合物生物合成通常受级联调控(cascade regulation),涉及簇内途径特异性调控蛋白[18],有时还受多效调控因子[19, 20]或全局调控因子[21, 22]的影响。然而随着研究的深入,越来越多的事实证明基因簇的激活受途径特异性激活蛋白直接控制,而高层调控因子感应各种环境以及生理信号,最终通过调控次级代谢簇中激活蛋白的表达间接控制生物合成。绝大多数基因簇内都存在这种底层激活蛋白。依据序列特征,它们又被分为不同类型,例如SARPs (Streptomyces antibiotic regulatory proteins)、ARR (Atypical response regulators)、LALs (Large ATP-binding regulators of the LuxR family)、 LTTR (LysR-type transcriptional regulators)等。其中SARPs在链霉菌中分布最为广泛并且研究更为深入,例如Streptomyces coelicolor A3(2)中II型聚酮Act合成簇内的ActII-ORF4[18],Streptomyces fradiae中I型聚酮泰乐菌素(tylosin)合成簇内的TylR[23],以及Streptomycin ambofaciens中II型聚酮醌那霉素(kinamycin)合成簇内的AlpV[24]等,这些SARP基因的缺失会使产生菌完全丧失聚酮合成能力,而过表达会导致聚酮产量显著提高[25]。例如,本课题组利用组成型强启动子kasOp*过表达S. coelicolor M145中Act合成簇SARP基因actII-orf4,该菌株在SMM和R2YE培养基中可分别提高产量至对照组的2.5和4.5倍[26]。广谱抗生素土霉素(oxytetracycline)是Streptomyces rimosus产生的II型聚酮,其合成基因簇中的SARP类调控蛋白OtcR 是土霉素合成基因簇的激活蛋白,为了提高土霉素产量,本课题组对S. rimosus M4108进行工程改造,当使用组成型强启动子SF14过表达两个串联的otcR基因时,成功得到土霉素高产菌株,该工程菌土霉素产量是出发菌株产量的6.49倍[27]。这些研究均表明,在链霉菌中过表达途径特异性激活蛋白,可以有效提高聚酮产量。同时这也暗示在实验室常规培养条件下这些SARPs在胞内的浓度远没有达到饱和,工业生产使用的诱变高产菌株也有可能通过过表达SARPs进一步提高聚酮合成能力。
链霉菌基因组中含有很多次级代谢产物生物合成基因簇(secondary metabolite biosynthesis gene clusters,BGCs),有产生多种次级代谢产物的潜力,例如S. coelicolor A3(2) 基因组中鉴定出至少29个BGCs[28],但是目前仅有少数次级代谢产物被发现,有很多BGCs在实验环境下并不转录表达,导致这些途径合成的终产物无法被鉴定和利用,这类基因簇被称为隐性生物合成基因簇。采用过表达途径特异性激活子的方法,可以激活隐性基因簇的表达,得到新的次级代谢产物。例如,研究者在Streptomyces ambofaciens ATCC 23877基因组中发现了一个巨大的隐性I型聚酮生物合成基因簇(包含25个基因,约150 kb),分析发现该基因簇中samR0484基因可能编码LAL类激活蛋白;为了得到该基因簇合成的产物,研究者使用组成型强启动子ermEp*过表达samR0484基因,成功分离得到I型聚酮stambomycins,发现该类化合物具有抗肿瘤活性[29]。该研究仅采用过表达激活蛋白的方法,便激活了整个庞大的生物合成基因簇,是一个成功的特例。
3 去除产物反馈抑制由于聚酮化合物大多都具有一定生物活性,如果在胞内过量积累也会对其产生菌自身生长带来影响或者会对其合成途径造成反馈抑制,从而限制其产量提高。ABC (ATP-binding cassette)转运蛋白可以将次级代谢产物排到胞外,解除其细胞毒性及反馈抑制,有效提高次级代谢产物产 量[30]。例如S. peucetius产生的II型聚酮DNR和DXR具有嵌入DNA的能力,当DNR和DXR在胞 内大量积累时,会抑制II型拓扑异构酶活性,同时也会对自身合成造成反馈抑制[10]。研究表明S. peucetius drrAB 编码的膜蛋白DrrA和DrrB具有类似于ABC转运蛋白的功能,两者协同发挥作用,可以将DNR、DXR及其结构类似物排到胞 外[31, 32, 33]。研究者在S. peucetius ATCC 27952中通过ermEp*过表达drrAB,增强DNR和DXR的外排,解除产物反馈抑制,从而使DNR和DXR产量相比野生菌分别提高3.2倍和2.2倍[34]。再例如Streptomyces avermitilis中阿维菌素生物合成基因簇上游的avtAB操纵子编码ABC转运蛋白,采用多拷贝质粒过表达avtAB,将阿维菌素排到胞外,可能缓解了 阿维菌素对自身合成途径的反馈抑制,最终使阿维菌素产量相比野生株提高2倍[35]。
除ABC转运蛋白外,链霉菌次级代谢基因簇中还普遍存在类似于tetR-tetA模型的外排泵基因,该模型中TetR为负调控蛋白,阻遏四环素(tetracycline)外排泵基因tetA的转录表达,当四环素与TetR结合时,解除其对tetA的阻遏,此时四环素被TetA排到胞外[36]。例如Streptomyces glaucescens中II型聚酮特曲霉素(tetracenomycin,TCM)基因簇内的tcmR和tcmA[37], Streptomyces virginiae中I型聚酮维及霉素(virginiamycin)基因簇内的varR和varS[38],S. coelicolor中Act基因簇内的actR和actA[39]等。S. coelicolor 中调控蛋白AtrA可以结合到actII-orf4启动子区,激活ActII-ORF4蛋白的表达[40]。Act通过结合AtrA蛋白,抑制其DNA结合活性,从而使ActII-ORF4表达量下调,最终导致Act产量降低[41],因此Act对其自身合成途径具有反馈抑制作用。在Act合成基因簇内,操纵子actAB编码Act外排泵ActA,但是actAB操纵子的表达受ActR阻遏[39]。直接敲除actR,解除其产物对外排泵基因的阻遏作用,实现外排泵基因过表达,增强Act外排,去除Act对自身合成途径的反馈抑制,使Act产量提高4~5倍[42]。以上研究表明,这种增强合成途径终产物外排的方法,可以有效解除产物反馈抑制,提高聚酮合成的产量。
4 强化前体供应前体物质是初级代谢和次级代谢的桥梁,例如,来自初级代谢的乙酰CoA、丙二酸单酰CoA、葡萄糖-6-磷酸、α-酮戊二酸、还原力NADPH、甲基丙二酸单酰CoA、乙基丙二酸单酰CoA、丙酰CoA等都可以作为次级代谢产物合成的前体或辅因子[43, 44, 45]。丙二酸单酰 CoA 是聚酮合成的重要前体,它不仅是聚酮碳链延伸的必需单元,也可作为聚酮合成起始单位,增强丙二酸单酰 CoA 合成有利于提高聚酮产量[46]。例如Act以乙酰CoA为起始,丙二酸单酰CoA为延伸单位进行生物合成[42]。研究者通过敲除S. coelicolor 中葡萄糖-6-磷酸脱氢酶,阻断磷酸戊糖途径,增强了糖酵解,使胞内积累较多的乙酰CoA,从而提高Act产量接近2倍[47];与此同时,使用ermEp*过表达乙酰CoA羧化酶复合体,使乙酰CoA高效转化为丙二酸单酰CoA,可以进一步提高Act产量近6倍[47]。
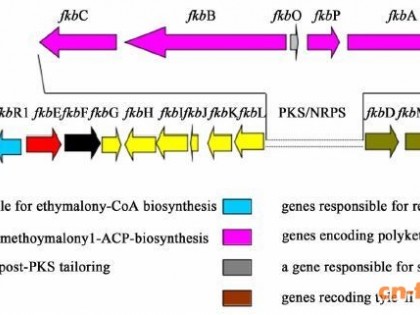
具有免疫抑制活性的I型聚酮FK506 (tacrolimus) 是Streptomyces tsukubaensis 和Streptomyces clavuligerus产生的次级代谢产物,其生物合成过程需要丙二酸单酰CoA、甲基丙二酸单酰CoA、methoxymalonyl (MOM)-ACP和allylmalonyl (AM)-CoA等多种延伸单位[48, 49]。研究者通过在R2YE培养基中外源添加10 mmol/L油酸甲酯,使野生株S. clavuligerus CKD1119胞内甲基丙二酸单酰CoA浓度提高12.5倍,同时FK506产量提高2.5倍(15 mg/L);将甲基丙二酸单酰CoA变位酶(methylmalonyl-CoA mutase,MCM)途径引入到S. clavuligerus CKD1119中,使胞内甲基丙二酸单酰 CoA浓度提高3倍,同时FK506产量提高1.5倍,通过在培养基中添加油酸甲酯,在胞内被MCM途径转化为甲基丙二酸单酰CoA,使FK506产量进一步提高2倍(17.8 mg/L)[48]。延伸单位MOM-ACP和AM-CoA在聚酮合成过程中较为罕见,通过在S. tsukubaensis中单独增加MOM-ACP和AM-CoA合成基因拷贝数,实现其合成基因过表达,与出发菌株相比,分别使FK506产量提高30%和100%[49]。 以上研究均表明,通过增加前体供应,可以在链霉菌中有效提高聚酮合成的产量。由于聚酮合成的前体物质同时也可能是初级代谢途径中的前体物质,例如乙酰CoA和丙二酸单酰 CoA也参与脂肪酸的合成,这种使用组成型启动子过表达乙酰CoA羧化酶所产生的丙二酸单酰 CoA,在稳定期以前并不能直接参与聚酮合成,从而限制聚酮产量提高[50]。
5 异源表达超级底盘构建在工业生产条件下,很多链霉菌菌种无法快速生长及高效合成抗生素。因此,开发通用的异源宿主是一种很好的解决办法。在异源表达BGCs时,链霉菌和大肠杆菌是两种最常用异源宿主[15]。而链霉菌相比大肠杆菌具有明显的优势,首先,很多BGCs本身就来源于链霉菌,其编码基因与链霉菌宿主有相同的密码子偏好性;另外,链霉菌宿主通常具有更全面的前体供应能力。
构建异源链霉菌底盘宿主时,最常用的策略是对宿主基因组进行简化,简化方法是在不影响宿主自身生长和目标产物合成的前提下,删除一些非必须基因或竞争途径基因,为目标产物合成提供更多的前体资源。例如,S. coelicolor M145 作为链霉菌模式菌株,主要产生4种抗生素,分别是Red (undecylprodigiosin)、CDA (calcium-dependent antibiotic)、I型聚酮coelimycin、II型聚酮Act[51, 52]。Act是S. coelicolor M145最主要的次级代谢产物[50],有着较高的产量,表明S. coelicolor M145可以为聚酮高效合成提供大量前体,因此研究者利用S. coelicolor构建链霉菌聚酮化合物异源生物合成的底盘菌株[50]。为了避免自身次级代谢产物合成途径与外源次级代谢产物合成途径对胞内前体的竞争,通过删除S. coelicolor M145中上述4种抗生素的生物合成基因簇,得到菌株S. coelicolor M1146;然后在RNA聚合酶β亚基RpoB和核糖体蛋白S12编码基因中引入点突变,分别得到菌株S. coelicolor M1152和菌株S. coelicolor M1154[52];进而在M1152的基础上删除3种内源的III型PKS基因簇,得到菌株S. coelicolor M1317[53],构建得到了一系列以S. coelicolor为底盘的次级代谢产物合成的异源宿主。FK506、III型聚酮germicidin和淡黄霉素等抗生素均在S. coelicolor异源底盘中得到了高效生物合成[53, 54, 55]。构建异源链霉菌底盘宿主时,最常用的策略是对宿主基因组进行简化,简化方法是在不影响宿主自身生长和目标产物合成的前提下,删除一些非必须基因或竞争途径基因,为目标产物合成提供更多的前体资源。例如,S. coelicolor M145 作为链霉菌模式菌株,主要产生4种抗生素,分别是Red (undecylprodigiosin)、CDA (calcium-dependent antibiotic)、I型聚酮coelimycin、II型聚酮Act[51, 52]。Act是S. coelicolor M145最主要的次级代谢产物[50],有着较高的产量,表明S. coelicolor M145可以为聚酮高效合成提供大量前体,因此研究者利用S. coelicolor构建链霉菌聚酮化合物异源生物合成的底盘菌株[50]。为了避免自身次级代谢产物合成途径与外源次级代谢产物合成途径对胞内前体的竞争,通过删除S. coelicolor M145中上述4种抗生素的生物合成基因簇,得到菌株S. coelicolor M1146;然后在RNA聚合酶β亚基RpoB和核糖体蛋白S12编码基因中引入点突变,分别得到菌株S. coelicolor M1152和菌株S. coelicolor M1154[52];进而在M1152的基础上删除3种内源的III型PKS基因簇,得到菌株S. coelicolor M1317[53],构建得到了一系列以S. coelicolor为底盘的次级代谢产物合成的异源宿主。FK506、III型聚酮germicidin和淡黄霉素等抗生素均在S. coelicolor异源底盘中得到了高效生物合成[53, 54, 55]。
S. avermitilis合成的主要次级代谢产物有菲律宾菌素(filipin)、阿维菌素、寡霉素(oligomycin),它们均由I型PKS合成[56]。转座突变、基因敲除等遗传操作方法已经在S. avermitilis 中成功建立,为其工程改造提供便利,同时S. avermitilis可以为次级代谢产物高效合成提供多种前体,因此也是一个较理想的BGCs异源表达宿主[57]。为了构建全能型次级代谢产物异源合成宿主,S. avermitilis基因组被人工精简,得到了一系列删除大量冗余基因的突变株SUKA2~SUKA22。例如同时删除菲律宾菌素、阿维菌素、寡霉素生物合成基因簇的突变株,通过进一步删除基因组上一些特定区域并增加一些标签基因,得到不产上述3种次级代谢产物的突变型菌株SUKA5[56]。具有抗癌活性的大环内酯类I型聚酮pladienolides是由Streptomyces platensis Mer-11107 产生的次级代谢产物[58, 59, 60]。将pladienolides生物合成基因簇分别克隆到S. avermitilis 野生型菌株和SUKA5 菌株中,同时使用组成型启动子ermEp表达pladienolides合成基因簇特异性激活子PldR,在SUKA5菌株中pladienolides 产量是野生型S. avermitilis产量的20倍[56]。此外,I型聚酮红霉素、巴菲霉素(bafilomycin)、金链菌素(aureothin),以及II型聚酮土霉素和抗霉素(resistomycin)等均在SUKA22菌株中成功实现异源合成[56, 57, 58, 59, 60, 61]。除此之外,其它链霉菌作为异源表达宿主也已经被成功构建和应用,例如Streptomyces albus J1074、S. ambofaciens BES2074、Streptomyces toyocaensis NRRL15009、Streptomyces cinnamonensis等都被应用于BGCs的异源表达[62]。
6 合成生物学策略随着高通量测序技术和生物信息学分析方法的不断发展,更多的BGCs被发现,为聚酮合成研究提供了便利。对大量BGCs分析发现,聚酮化合物BGCs在基因簇组织方式上是高度模块化的,这一特点便于采用合成生物学方法对其进行基因水平再编辑,来提高聚酮合成产量或者发现新的聚酮化合物[4]。利用合成生物学方法,在不改变结构基因编码功能的前提下,对BGCs内的结构基因进行重排;去除原始的顺式和反式调控元件,引入新的、可控制的调控系统来调节次级代谢产物的生物合成。例如,具有抗病毒和抗疟疾活性的spectinabilin 是Streptomyces spectabilis和Streptomyces orinoci 产生的I型聚酮[63]。当在Streptomyces lividans 中异源表达来自S. orinoci的spectinabilin生物合成基因簇时,没有得到预期产物。研究者采用合成生物学方法,对spectinabilin 生物合成基因簇进行重排,将基因簇分成3个模块:启动子模块、基因模块和辅助模块[64]。在启动子模块中,使用S. lividans持家基因强启动子,来启动外源基因的转录,以确保外源基因簇在S. lividans中表达;在辅助模块中,引入可以维持外源DNA在宿主内复制和筛选的元件;基因模块包含了spectinabilin生物合成所需的8个基因。 最后,将重新编辑的、人工合成得到的基因簇克隆到启动子模块中启动子下游,导入S. lividans。在重新编辑的基因簇中,原基因簇的复杂调控被解除,取而代之的是可预测的、易控制的调控系统,成功实现了spectinabilin在S. lividans中的异源合成,产量达到100 μg/L[64]。该研究表明,在链霉菌中,可以有效利用合成生物学策略进行隐性基因簇激活并获得相应产物。目前,链霉菌中已经积累了大量可被合成生物学操作利用的元件,例如启动子[65, 66, 67]、RBS (ribosomal binding site)[67]和整合质粒[68, 69]等,为进一步提高产量、开发新的具有应用价值的聚酮化合物奠定基础。
7 展 望聚酮化合物作为天然产物中最大的一类,具有重要的生物活性和应用价值。链霉菌属具有较强的聚酮生物合成能力,但野生型链霉菌聚酮合成产量远远不能达到工业化生产规模的需求。传统的代谢工程操作,例如过表达合成途径中的限速酶、阻断竞争代谢途径、解除反馈抑制等方法,虽然可以提高目标化合物产量,但是由于细胞代谢的复杂性,会造成胞内酶水平失衡,使细胞积累过量的酶或者中间产物,对细胞造成毒害,最终抑制细胞生长或阻碍目标化合物产量的提高[70]。利用合成生物学策略,通过对合成过程中关键节点进行智能控制,可以有效解决传统代谢工程操作带来的弊端,使目标产物高效合成。例如,早期使用能够响应乙酰磷酸浓度的调控元件来调节番茄素生物合成[71]。再例如Keasling研究组在进行amorphadiene异源生物合成时,使用Escherichia coli中天然存在的响应有毒中间代谢物FPP的生理启动子控制下游途径合成,实现E. coli细胞胞内FPP浓度自我调节和平衡下游合成途径[72]。此外,近年在E. coli中利用动态感应调控系统(dynamic sensor-regulator system,DSRS)提高生物柴油(fatty acid ethyl ester,FAEE)和脂肪酸(fatty acids,FA)产量取得了丰硕成果。例如,采用响应fatty acyl-CoA的调控蛋白FadR来控制FAEE合成途径中关键酶的表达,实现胞内代谢流平衡,避免中间产物乙醇和fatty acyl-CoA在细胞内过度积累,该方法得到的高产菌株与之前工程化的菌株相比,FAEE产量提高3倍[73, 74]。丙二酸单酰CoA是FA、聚酮等重要化合物生物合成的前体,乙酰CoA羧化酶复合体催化乙酰CoA生成丙二酸单酰CoA,是FA和聚酮合成的限速步骤。在E. coli中过表达乙酰CoA羧化酶复合体,虽然可以提高FA产量,但是降低了细胞生长速度[75, 76]。研究者将来自Bacillus subtilis 的FapR蛋白导入到E. coli中来感应胞内丙二酸单酰CoA浓度,人工构建了受FapR蛋白激活和阻遏的两个启动子,用这两个启动子分别控制乙酰CoA羧化酶复合体和脂肪酸合酶基因的转录表达,动态调节胞内丙二酸单酰CoA浓度,使丙二酸单酰CoA高效地流向FA合成途径,与野生菌相比,FA产量提高15.7倍[77]。这些研究充分表明,在工程改造过程中,通过表达控制元件对相关生物合成途径关键节点进行动态、精细调控,实现关键基因“适时”、“适量”表达,能够显著提高目标产物生物合成能力。
链霉菌生长具有复杂的形态和发育分化周期,以及从初级代谢到次级代谢的转折,而聚酮化合物都是次级代谢的产物,因此聚酮在链霉菌完成初级生长后才启动合成。这一合成时序对聚酮产生菌具有重要的生物学意义:聚酮作为抗生素,其靶点一般为重要生命过程的关键环节,如细胞壁合成、RNA转录,蛋白质翻译等,如果在菌体生长对数期或更早的生长时期开启合成,势必对菌体生长造成不利的影响;另外,聚酮作为次级代谢产物,不为菌体生长所必须。所以,在实际生产过程中,应该充分利用聚酮在稳定期开始大量合成这一自然进化特征,而不是人为的通过简单过表达相关基因来提前启动聚酮生物合成。因此,我们希望今后在链霉菌工程改造中,借助合成生物学策略,通过在链霉菌中加载人工设计的控制元件,对聚酮化合物生物合成途径关键节点进行智能调控,实现关键基因“适时”、“适量”表达,来显著提高链霉菌中聚酮化合物生物合成能力。例如图 2所示,构建一个通过感应细胞生长来开启前体供应的调控模块,当链霉菌生长到稳定期时开启聚酮前体合成和供应;同时构建聚酮合成动态感应调控系统,可以根据前体浓度来微调合成途径中特异性激活蛋白表达,从而调节聚酮合成基因簇表达,实现聚酮生物合成智能动态控制,提高聚酮合成产量。我们相信,通过设计和开发智能人工控制系统,可以在链霉菌中大幅提高聚酮生物合成能力,为聚酮化合物工业生产提供最优的解决方案。
 |
| 图 2. 合成生物学策略理性适配聚酮生物合成相关途径 Figure 2. Synthetic biology strategies to dynamically adjust the metabolic fluxes of pathways related to polyketide synthesis. |
|
图选项
|
| [1] | Deng Z, Bai L. Antibiotic biosynthetic pathways and pathway engineering——a growing research field in China. Natural Product Reports, 2006, 23(5): 811-827. |
| [2] | Staunton J, Weissman KJ. Polyketide biosynthesis: a millennium review. Natural Product Reports, 2001, 18(4): 380-416. |
| [3] | Weissman KJ, Leadlay PF. Combinatorial biosynthesis of reduced polyketides. Nature Reviews. Microbiology, 2005, 3(12): 925-936. |
| [4] | Cummings M, Breitling R, Takano E. Steps towards the synthetic biology of polyketide biosynthesis. FEMS Microbiology Letters, 2014, 351(2): 116-125. |
| [5] | Park SR, Yoo YJ, Ban YH, Yoon YJ. Biosynthesis of rapamycin and its regulation: past achievements and recent progress. The Journal of Antibiotics (Tokyo), 2010, 63(8): 434-441. |
| [6] | Baginski M, Czub J. Amphotericin B and its new derivatives-mode of action. Current Drug metabolism, 2009, 10(5): 459-469. |
| [7] | Pitterna T, Cassayre J, Huter OF, Jung PM, Maienfisch P, Kessabi FM, Quaranta L, Tobler H. New ventures in the chemistry of avermectins. Bioorganic & Medicinal Chemistry, 2009, 17(12): 4085-4095. |
| [8] | Hertweck C, Luzhetskyy A, Rebets Y, Bechthold A. Type II polyketide synthases: gaining a deeper insight into enzymatic teamwork. Natural Product Reports, 2007, 24(1): 162-190. |
| [9] | Keatinge-Clay AT, Maltby DA, Medzihradszky KF, Khosla C, Stroud RM. An antibiotic factory caught in action. Nature Structural & Molecular Biology, 2004, 11(9): 888-893. |
| [10] | Vasanthakumar A, Kattusamy K, Prasad R. Regulation of daunorubicin biosynthesis in Streptomyces peucetius-feed forward and feedback transcriptional control. Journal of Basic Microbiology, 2013, 53(8): 636-644. |
| [11] | Tacar O, Sriamornsak P, Dass CR. Doxorubicin: an update on anticancer molecular action, toxicity and novel drug delivery systems. The Journal of Pharmacy and Pharmacology, 2013, 65(2): 157-170. |
| [12] | Li Y, Muller R. Non-modular polyketide synthases in myxobacteria. Phytochemistry, 2009, 70(15-16): 1850-1857. |
| [13] | Yu D, Xu F, Zeng J, Zhan J. Type III polyketide synthases in natural product biosynthesis. IUBMB Life, 2012, 64(4): 285-295. |
| [14] | Ghimire GP, Oh TJ, Liou K, Sohng JK. Identification of a cryptic type III polyketide synthase (1,3,6,8-tetrahydroxynaphthalene synthase) from Streptomyces peucetius ATCC 27952. Molecules and Cells, 2008, 26(4): 362-367. |
| [15] | Pickens LB, Tang Y, Chooi YH. metabolic engineering for the production of natural products. Annual Review of Chemical and Biomolecular Engineering, 2011, 2: 211-236. |
| [16] | Jiang H, Wang YY, Ran XX, Fan WM, Jiang XH, Guan WJ, Li YQ. Improvement of natamycin production by engineering of phosphopantetheinyl transferases in Streptomyces chattanoogensis L10. Applied and Environmental Microbiology, 2013, 79(11): 3346-3354. |
| [17] | Malla S, Niraula NP, Liou K, Sohng JK. Enhancement of doxorubicin production by expression of structural sugar biosynthesis and glycosyltransferase genes in Streptomyces peucetius. Journal of Bioscience and Bioengineering, 2009, 108(2): 92-98. |
| [18] | Fernandez-Moreno MA, Caballero JL, Hopwood DA, Malpartida F. The act cluster contains regulatory and antibiotic export genes, direct targets for translational control by the bldA tRNA gene of Streptomyces. Cell, 1991, 66(4): 769-780. |
| [19] | Horinouchi S, Beppu T. Hormonal control by A-factor of morphological development and secondary metabolism in Streptomyces. Proceedings of the Japan Academy. Series B, Physical and Biological Sciences, 2007, 83(9/10): 277-295. |
| [20] | Rigali S, Titgemeyer F, Barends S, Mulder S, Thomae AW, Hopwood DA, van Wezel GP. Feast or famine: the global regulator DasR links nutrient stress to antibiotic production by Streptomyces. EMBO Reports, 2008, 9(7): 670-675. |
| [21] | Allenby NE, Laing E, Bucca G, Kierzek AM, Smith CP. Diverse control of metabolism and other cellular processes in Streptomyces coelicolor by the PhoP transcription factor: genome-wide identification of in vivo targets. Nucleic Acids Research, 2012, 40(19): 9543-9556. |
| [22] | McKenzie NL, Nodwell JR. Phosphorylated AbsA2 negatively regulates antibiotic production in Streptomyces coelicolor through interactions with pathway-specific regulatory gene promoters. Journal of Bacteriology, 2007, 189(14): 5284-5292. |
| [23] | Bate N, Stratigopoulos G, Cundliffe E. Differential roles of two SARP-encoding regulatory genes during tylosin biosynthesis. Molecular Microbiology, 2002, 43(2): 449-458. |
| [24] | Aigle B, Pang X, Decaris B, Leblond P. Involvement of AlpV, a new member of the Streptomyces antibiotic regulatory protein family, in regulation of the duplicated type II polyketide synthase alp gene cluster in Streptomyces ambofaciens. Journal of Bacteriology, 2005, 187(7): 2491-2500. |
| [25] | Hung TV, Malla S, Park BC, Liou K, Lee HC, Sohng JK. Enhancement of clavulanic acid by replicative and integrative expression of ccaR and cas2 in Streptomyces clavuligerus NRRL3585. Journal of Microbiology and Biotechnology, 2007, 17(9): 1538-1545. |
| [26] | Wang W, Li X, Wang J, Xiang S, Feng X, Yang K. An engineered strong promoter for streptomycetes. Applied and Environmental Microbiology, 2013, 79(14): 4484-4492. |
| [27] | Yin S, Wang W, Wang X, Zhu Y, Jia X, Li S, Yuan F, Zhang Y, Yang K. Identification of a cluster-situated activator of oxytetracycline biosynthesis and manipulation of its expression for improved oxytetracycline production in Streptomyces rimosus. Microbial Cell Factories, 2015, 14: 46. |
| [28] | Liu G, Chater KF, Chandra G, Niu G, Tan H. Molecular regulation of antibiotic biosynthesis in streptomyces. Microbiology and Molecular Biology Reviews : MMBR, 2013, 77(1): 112-143. |
| [29] | Laureti L, Song L, Huang S, Corre C, Leblond P, Challis GL, Aigle B. Identification of a bioactive 51-membered macrolide complex by activation of a silent polyketide synthase in Streptomyces ambofaciens. Proceedings of the National Academy of Sciences of the United States of America, 2011, 108(15): 6258-6263. |
| [30] | Martin JF, Casqueiro J, Liras P. Secretion systems for secondary metabolites: how producer cells send out messages of intercellular communication. Current Opinion in Microbiology, 2005, 8(3): 282-293. |
| [31] | Srinivasan P, Palani SN, Prasad R. Daunorubicin efflux in Streptomyces peucetius modulates biosynthesis by feedback regulation. FEMS Microbiology Letters, 2010, 305(1): 18-27. |
| [32] | Li W, Sharma M, Kaur P. The DrrAB efflux system of Streptomyces peucetius is a multidrug transporter of broad substrate specificity. The Journal of Biological Chemistry, 2014, 289(18): 12633-12646. |
| [33] | Kaur P, Rao DK, Gandlur SM. Biochemical characterization of domains in the membrane subunit DrrB that interact with the ABC subunit DrrA: identification of a conserved motif. Biochemistry, 2005, 44(7): 2661-2670. |
| [34] | Malla S, Niraula NP, Liou K, Sohng JK. Self-resistance mechanism in Streptomyces peucetius: overexpression of drrA, drrB and drrC for doxorubicin enhancement. Microbiological Research, 2010, 165(4): 259-267. |
| [35] | Qiu J, Zhuo Y, Zhu D, Zhou X, Zhang L, Bai L, Deng Z. Overexpression of the ABC transporter AvtAB increases avermectin production in Streptomyces avermitilis. Applied Microbiology and Biotechnology, 2011, 92(2): 337-345. |
| [36] | Hillen W, Berens C. Mechanisms underlying expression of Tn10 encoded tetracycline resistance. Annual Review of Microbiology, 1994, 48: 345-369. |
| [37] | Guilfoile PG, Hutchinson CR. The Streptomyces glaucescens TcmR protein represses transcription of the divergently oriented tcmR and tcmA genes by binding to an intergenic operator region. Journal of Bacteriology, 1992, 174(11): 3659-3666. |
| [38] | Namwat W, Lee CK, Kinoshita H, Yamada Y, Nihira T. Identification of the varR gene as a transcriptional regulator of virginiamycin S resistance in Streptomyces virginiae. Journal of Bacteriology, 2001, 183(6): 2025-2031. |
| [39] | Tahlan K, Ahn SK, Sing A, Bodnaruk TD, Willems AR, Davidson AR, Nodwell JR. Initiation of actinorhodin export in Streptomyces coelicolor. Molecular Microbiology, 2007, 63(4): 951-961. |
| [40] | Uguru GC, Stephens KE, Stead JA, Towle JE, Baumberg S, McDowall KJ. Transcriptional activation of the pathway-specific regulator of the actinorhodin biosynthetic genes in Streptomyces coelicolor. Molecular Microbiology, 2005, 58(1): 131-150. |
| [41] | Li X, Yu T, He Q, McDowall KJ, Jiang B, Jiang Z, Wu L, Li G, Li Q, Wang S, Shi Y, Wang L, Hong B. Binding of a biosynthetic intermediate to AtrA modulates the production of lidamycin by Streptomyces globisporus. Molecular Microbiology, 2015, 96(6): 1257-1271. |
| [42] | Xu Y, Willems A, Au-Yeung C, Tahlan K, Nodwell JR. A two-step mechanism for the activation of actinorhodin export and resistance in Streptomyces coelicolor. MBio, 2012, 3(5): e00191-00112. |
| [43] | Rokem JS, Lantz AE, Nielsen J. Systems biology of antibiotic production by microorganisms. Natural Product Reports, 2007, 24(6): 1262-1287. |
| [44] | Chan YA, Podevels AM, Kevany BM, Thomas MG. Biosynthesis of polyketide synthase extender units. Natural Product Reports, 2009, 26(1): 90-114. |
| [45] | Blazic M, Kosec G, Baebler S, Gruden K, Petkovic H. Roles of the crotonyl-CoA carboxylase/reductase homologues in acetate assimilation and biosynthesis of immunosuppressant FK506 in Streptomyces tsukubaensis. Microbial Cell Factories, 2015, 14(1): 164. |
| [46] | Maharjan S, Park JW, Yoon YJ, Lee HC, Sohng JK. metabolic engineering of Streptomyces venezuelae for malonyl-CoA biosynthesis to enhance heterologous production of polyketides. Biotechnology Letters, 2010, 32(2): 277-282. |
| [47] | Ryu YG, Butler MJ, Chater KF, Lee KJ. Engineering of primary carbohydrate metabolism for increased production of actinorhodin in Streptomyces coelicolor. Applied and Environmental Microbiology, 2006, 72(11): 7132-7139. |
| [48] | Mo S, Ban YH, Park JW, Yoo YJ, Yoon YJ. Enhanced FK506 production in Streptomyces clavuligerus CKD1119 by engineering the supply of methylmalonyl-CoA precursor. Journal of Industrial Microbiology & Biotechnology, 2009, 36(12): 1473-1482. |
| [49] | Chen DD, Zhang Q, Zhang QL, Cen PL, Xu ZN, Liu W. Improvement of FK506 production in Streptomyces tsukubaensis by genetic enhancement of the supply of unusual polyketide extender units via utilization of two distinct site-specific recombination systems. Applied and Environmental Microbiology, 2012, 78(15): 5093-5103. |
| [50] | Coze F, Gilard F, Tcherkez G, Virolle MJ, Guyonvarch A. Carbon-flux distribution within Streptomyces coelicolor metabolism: a comparison between the actinorhodin-producing strain M145 and its non-producing derivative M1146. PLoS One, 2013, 8(12): e84151. |
| [51] | Borodina I, Krabben P, Nielsen J. Genome-scale analysis of Streptomyces coelicolor A3(2) metabolism. Genome Research, 2005, 15(6): 820-829. |
| [52] | Gomez-Escribano JP, Bibb MJ. Engineering Streptomyces coelicolor for heterologous expression of secondary metabolite gene clusters. Microbial Biotechnology, 2011, 4(2): 207-215. |
| [53] | Thanapipatsiri A, Claesen J, Gomez-Escribano JP, Bibb M, Thamchaipenet A. A Streptomyces coelicolor host for the heterologous expression of Type III polyketide synthase genes. Microbial Cell Factories, 2015, 14: 145. |
| [54] | Jones AC, Gust B, Kulik A, Heide L, Buttner MJ, Bibb MJ. Phage p1-derived artificial chromosomes facilitate heterologous expression of the FK506 gene cluster. PLoS One, 2013, 8(7): e69319. |
| [55] | Gomez-Escribano JP, Bibb MJ. Heterologous expression of natural product biosynthetic gene clusters in Streptomyces coelicolor: from genome mining to manipulation of biosynthetic pathways. Journal of Industrial Microbiology & Biotechnology, 2014, 41(2): 425-431. |
| [56] | Komatsu M, Uchiyama T, Omura S, Cane DE, Ikeda H. Genome-minimized Streptomyces host for the heterologous expression of secondary metabolism. Proceedings of the National Academy of Sciences of the United States of America, 2010, 107(6): 2646-2651. |
| [57] | Ikeda H, Kazuo SY, Omura S. Genome mining of the Streptomyces avermitilis genome and development of genome-minimized hosts for heterologous expression of biosynthetic gene clusters. Journal of Industrial Microbiology & Biotechnology, 2014, 41(2): 233-250. |
| [58] | Sakai T, Asai N, Okuda A, Kawamura N, Mizui Y. Pladienolides, new substances from culture of Streptomyces platensis Mer-11107. II. Physico-chemical properties and structure elucidation. The Journal of Antibiotics (Tokyo), 2004, 57(3): 180-187. |
| [59] | Mizui Y, Sakai T, Iwata M, Uenaka T, Okamoto K, Shimizu H, Yamori T, Yoshimatsu K, Asada M. Pladienolides, new substances from culture of Streptomyces platensis Mer-11107. III. In vitro and in vivo antitumor activities. The Journal of Antibiotics (Tokyo), 2004, 57(3): 188-196. |
| [60] | Machida K, Arisawa A, Takeda S, Tsuchida T, Aritoku Y, Yoshida M, Ikeda H. Organization of the biosynthetic gene cluster for the polyketide antitumor macrolide, pladienolide, in Streptomyces platensis Mer-11107. Bioscience, Biotechnology, and Biochemistry, 2008, 72(11): 2946-2952. |
| [61] | Komatsu M, Komatsu K, Koiwai H, Yamada Y, Kozone I, Izumikawa M, Hashimoto J, Takagi M, Omura S, Shin-ya K, Cane DE, Ikeda H. Engineered Streptomyces avermitilis host for heterologous expression of biosynthetic gene cluster for secondary metabolites. ACS Synthetic Biology, 2013, 2(7): 384-396. |
| [62] | Baltz RH. Genetic manipulation of secondary metabolite biosynthesis for improved production in Streptomyces and other actinomycetes. Journal of Industrial Microbiology & Biotechnology, 2015: 1-28. |
| [63] | Choi YS, Johannes TW, Simurdiak M, Shao Z, Lu H, Zhao H. Cloning and heterologous expression of the spectinabilin biosynthetic gene cluster from Streptomyces spectabilis. Molecular BioSystems, 2010, 6(2): 336-338. |
| [64] | Shao Z, Rao G, Li C, Abil Z, Luo Y, Zhao H. Refactoring the silent spectinabilin gene cluster using a plug-and-play scaffold. ACS Synthetic Biology, 2013, 2(11): 662-669. |
| [65] | Luo Y, Zhang L, Barton KW, Zhao H. Systematic identification of a panel of strong constitutive promoters from Streptomyces albus. ACS Synthetic Biology, 2015, 4(9): 1001-1010. |
| [66] | Li S, Wang J, Li X, Yin S, Wang W, Yang K. Genome-wide identification and evaluation of constitutive promoters in streptomycetes. Microbial Cell Factories, 2015, 14(1): 172. |
| [67] | Bai C, Zhang Y, Zhao X, Hu Y, Xiang S, Miao J, Lou C, Zhang L. Exploiting a precise design of universal synthetic modular regulatory elements to unlock the microbial natural products in Streptomyces. Proceedings of the National Academy of Sciences of the United States of America, 2015, 112(39): 12181-12186. |
| [68] | Herrmann S, Siegl T, Luzhetska M, Petzke L, Jilg C, Welle E, Erb A, Leadlay PF, Bechthold A, Luzhetskyy A. Site-specific recombination strategies for engineering actinomycete genomes. Applied and Environmental Microbiology, 2012, 78(6): 1804-1812. |
| [69] | Fayed B, Ashford DA, Hashem AM, Amin MA, El Gazayerly ON, Gregory MA, Smith MC. Multiplexed integrating plasmids for engineering of the erythromycin gene cluster for expression in Streptomyces spp. and combinatorial biosynthesis. Applied and Environmental Microbiology, 2015, 81(24): 8402-8413. |
| [70] | Pitera DJ, Paddon CJ, Newman JD, Keasling JD. Balancing a heterologous mevalonate pathway for improved isoprenoid production in Escherichia coli. metabolic Engineering, 2007, 9(2): 193-207. |
| [71] | Farmer WR, Liao JC. Improving lycopene production in Escherichia coli by engineering metabolic control. Nature Biotechnology, 2000, 18(5): 533-537. |
| [72] | Dahl RH, Zhang F, Alonso-Gutierrez J, Baidoo E, Batth TS, Redding-Johanson AM, Petzold CJ, Mukhopadhyay A, Lee TS, Adams PD, Keasling JD. Engineering dynamic pathway regulation using stress-response promoters. Nature Biotechnology, 2013, 31(11): 1039-1046. |
| [73] | Steen EJ, Kang Y, Bokinsky G, Hu Z, Schirmer A, McClure A, Del Cardayre SB, Keasling JD. Microbial production of fatty-acid-derived fuels and chemicals from plant biomass. Nature, 2010, 463(7280): 559-562. |
| [74] | Zhang F, Carothers JM, Keasling JD. Design of a dynamic sensor-regulator system for production of chemicals and fuels derived from fatty acids. Nature Biotechnology, 2012, 30(4): 354-359. |
| [75] | Davis MS, Solbiati J, Cronan JE, Jr. Overproduction of acetyl-CoA carboxylase activity increases the rate of fatty acid biosynthesis in Escherichia coli. The Journal of Biological Chemistry, 2000, 275(37): 28593-28598. |
| [76] | Zha W, Rubin-Pitel SB, Shao Z, Zhao H. Improving cellular malonyl-CoA level in Escherichia coli via metabolic engi- neering. metabolic Engineering, 2009, 11(3): 192-198. |
| [77] | Xu P, Li L, Zhang F, Stephanopoulos G, Koffas M. Improving fatty acids production by engineering dynamic pathway regulation and metabolic control. Proceedings of the National Academy of Sciences of the United States of America, 2014, 111(31): 11299-11304. |