培养某一类型细胞没有固定的培养条件。在MEM中培养的细胞,很可能在DMEM或M199中同样很容易生长。总之,首选MEM做粘附细胞培养、 RPMI-1640做悬浮细胞培养是一个好的开始。
2.何时须更换培养基?
视细胞生长密度而定,或遵照细胞株基本资料上之更换时间,按时更换培养基即可。
3.可否使用与原先培养条件不同之培养基?
不能。每一细胞株均有其特定使用且已适应之细胞培养基,若骤然使用和原先提供之培养条件不同之培养基,细胞大都无法立即适应,造成细胞无法存活。
4.培养细胞时应使用5 %或10% CO2?或根本没有影响?
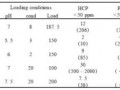
一般培养基中大都使用HCO3-/CO32-/H+作为pH的缓冲系统,而培养基中NaHCO3的含量将决定细胞培养时应使用的CO2浓度。当培养基中NaHCO3含量为每公升3.7 g时,细胞培养时应使用10 % CO2;当培养基中NaHCO3为每公升1.5 g时,则应使用5 % CO2培养细胞。
5.冷冻管应如何解冻?
取出冷冻管后,须立即放入37°C水槽中快速解冻,轻摇冷冻管使其在1分钟内全部融化,并注意水面不可超过冷冻管盖沿,否则易发生污染情形。另冷冻管由液氮桶中取出解冻时,必须注意安全,预防冷冻管之爆裂。
6. 怎样离心回收细胞?
欲回收动物细胞,其离心速率一般为300xg (约1000rpm),5 - 10分钟,过高之转速,将造成细胞死亡。
7.细胞冷冻培养基之成份为何?
动物细胞冷冻保存时最常使用的冷冻培养基是含5 - 10 %DMSO (dimethyl sulfoxide)和90 - 95 %原来细胞生长用之新鲜培养基均匀混合之。注意:由于 DMSO稀释时会放出大量热能,故不可将DMSO直接加入细胞液中,必须使用前先行配制完成。
8.应如何避免细胞污染?
细胞污染的种类可分成细菌、酵母菌、霉菌、病毒和霉浆菌。主要的污染原因为无菌操作技术不当、操作室环境不佳、污染之血清和污染之细胞等。严格之无菌操作技术、清洁的环境、与品质良好之细胞来源和培养基配制是减低污染之最好方法。
9.购买之细胞冷冻管经解冻后,为何会发生细胞数目太少之情形?
研究人员在冷冻细胞之培养时出现细胞数目太少,大都是因为离心过程操作上的失误,造成细胞的物理性损伤,以及细胞流失。建议细胞解冻后不要立刻离心,应待细胞生长隔夜后再更换培养基即可。
10.购买之细胞死亡或细胞存活率不佳可能原因?
研究人员在细胞培养时出现存活率不佳,常见原因可归纳为:培养基使用错误或培养基品质不佳。血清使用错误或血清的品质不佳。解冻过程错误。冷冻细胞解冻后,加以洗涤细胞和离心。悬浮细胞误认为死细胞。培养温度使用错误。细胞置于–80 °C太久。
11.什么培养基中可以省去加酚红?
酚红在培养基中用作PH值的指示剂:中性时为红色,酸性时为黄色,碱性时为紫色。研究表明,酚红可以模拟固醇类激素的作用,(特别是雌激素)。为避免固醇类反应,培养细胞,尤其是哺乳类细胞时,用不加酚红的培养基。由于酚红干扰检测,一些研究人员在做流式细胞检测时,不使用加有酚红的培养基。
一、如何选用培养基?
选择培养基没有一定标准,有几点建议可供参考:
建立某种细胞株所用的培养基应该是培养这种细胞首选的培养基。可以查阅文献,或在购买细胞株时咨询。
本单位惯用的培养基不妨一试,许多培养基可以适合多种细胞。
根据细胞株的特点、实验的需要来选择培养基。如小鼠细胞株多选1640;进行细胞杂交、基因转移实验,可选择IMDM。
用多种培养基培养目的细胞,观察其生长状态,可以用生长曲线、集落形成率等指标判断,根据实验结果选择最佳培养基,这是最客观的方法,但比较繁琐。
二、选择便宜的培养基品种成本就低吗?
通常,培养基可以适合多种细胞,细胞也可以在不同培养液中生长;例如在MEM中培养的细胞,很可能在DMEM或M199中同样很容易生长。
培养基养份不同会导致细胞生长效果不同,病毒或蛋白表达不同,应该选择效果最好的培养基,考虑生物制品的综合成本;
最终目的是追求生物制品的得率——得率高则成本低。
三、L-谷氨酰胺在细胞培养中重要吗?它在溶液中不稳定吗?
四、为什么培养基中可以省去酚红?
五、在新鲜培养基中添加了血清和抗生素后,有效期是多长?
六、为什么不要用碳酸氢钠调pH值?
DMEM(HED)培养基
MEM培养基
七、细胞生长质量很好,为什么病毒、蛋白表达量没有提高?
八、污染是培养基质量不好引起的吗?
培养基不是无菌产品,但有菌落数量控制。
培养基在使用前通过高压或过滤灭菌。
防止污染应该注意以下事项:
A.从污染的源头开始
确认工作细胞库是否被污染:用细菌、真菌及支原体无菌试验来确认并排除。同时要对无菌试验培养基的灵敏度进行验证。
确认毒种工作种子批是否被污染:用细菌、真菌及支原体无菌试验来确认并排除。同时要对无菌试验培养基的灵敏度进行验证。
确认所用培养基及其添加成分(如小牛血清、NaHCO3等)是否被污染:用细菌、真菌及支原体无菌试验来确认并排除。同时要对无菌试验培养基的灵敏度进行验证。实际生产中,可以从配制好的培养液中取少量加入营养琼脂于恒温培养箱内培养,48小时即可观察有无污染。
一些单位在使用血清时候往往不经过过滤除菌处理便直接加入到培养液中,可能带来污染。
其它:高压灭菌设备、过滤除菌设备均应进行验证,确保灭菌和除菌效果;前者应在投产前及其后的每6个月进行验证,后者应在每次除菌前、后进行验证工作(至少应在除菌后进行一次)。
另外,应将有毒区与无毒区严格分开,并有各自独立的空气净化系统及孵室,有毒区对无毒区应保持相对负压,防止病毒对培养细胞(尤其是细胞库)的污染。
B.
每二周(或每周)对无菌操作室及洁净区域按GMP要求进行检测
人员的GMP管理和无菌操作强化培训
C.
细菌的大小从0.1-700μm,为防止细小细菌