李思梦1,李晓静2,陈涛1
投稿时间: 2014-04-01
1 天津大学化工学院教育部系统生物工程重点实验室,天津300072
2 海军工程大学勤务学院,天津300072
李思梦, 李晓静, 陈涛. 代谢工程方法改造大肠杆菌生产胸苷. 生物工程学报, 2015, 31(1): 105–114.
Li SM, Li XJ, Chen T. metabolic engineering of Escherichia coli for thymidine production. Chin J Biotech, 2015, 31(1): 105–114.
对大肠杆菌Escherichia coli BL21 (DE3) 生物合成胸苷进行了研究。通过敲除E. coli BL21 嘧啶回补途径的deoA、tdk 和udp 三个基因,BS03 工程菌株能够积累21.6 mg/L 胸苷。为了增加合成胸苷前体物核糖-5-磷酸和NADPH 的供给,进一步敲除pgi 和pyrL 使工程菌BS05 胸苷的产量提高到90.5 mg/L。而通过过表达胸苷合成途径的ushA、thyA、dut、ndk、nrdA 和nrdB 六个基因,菌株BS08 胸苷的产量能达到272 mg/L。通过分批补料发酵,BS08 最终可以积累1 248.8 mg/L 的胸苷。本研究结果表明经过代谢工程改造的E. coli BL21 具有良好的胸苷合成能力和应用潜力。
关键词:代谢工程,胸苷,从头合成途径
胸苷包括一分子 2-脱氧核糖和一分子胸腺 嘧啶碱基,是抗艾滋病司他夫定 (3′-脱氧-2′,3′- 双脱氢胸苷) 和叠氮胸苷的前体物质[1-2]。由于 艾滋病病人数量的急剧增加,廉价的、能大规 模生产胸苷的工艺方法得到了广泛的关注。用 化学合成法生产胸苷,工艺过程十分冗长使得 最终得到的胸苷成本较为昂贵[3-5]。使用生物法 生产胸苷具有工艺简单、后续分离成本低廉等 优势,因此构建高产胸苷的工程菌株具有良好 的应用前景。
目前,国内 多是用菌种 诱变[6]来提 高胸苷的生产水平 或酶法 [5,7-8] 来生产胸苷 。在细胞 中,胸苷的用途仅涉及到 DNA 的合成,因此 细胞内胸苷的含量非常低,并且受到严密的调 控[9-12]。作为 DNA 的组成物质,嘧啶核苷酸 在微生物细胞内的合成有 2 种途径:一条是利 用葡萄糖等碳源和氮源合成核苷酸,这种合成 途径称为从头合成途径 (de novo pathway),另 一条是由 嘧 啶碱基通 过 核糖基化 及 磷酸化而 合成的补救途径。补救途径是细胞摄取环境中 的碱基和核苷来合成核苷酸,在这个过程中, 需要胸苷磷酸化酶、胸苷激酶和尿苷磷酸化酶 参与催化,这 3 种酶分别由 deoA 、tdk 和 udp 基因编码[13]。从头合成途径是从氨甲酰磷酸与
天冬氨酸合成氨甲酰磷酸天冬氨酸开始,经过 一 系列反应合成 UMP 。UMP 是嘧啶核苷酸的 共同前体,它经过一系列反应生成胞嘧啶核苷 酸和胸腺 嘧 啶核苷酸 。 在野生菌 中 ,前体物 dUMP 被直接转化成 dTMP ,进而生成 dTDP 和 dTTP 。胸苷在胞内的主要存在形式是 dTTP , 而且 dTTP 一经合成就马上被利用合成 DNA [14]。 目前通过 代 谢工程方 法 构建胸苷 生 产菌株的 研究较少,其中 Lee 课题组对大肠杆菌生产胸 苷进行了较系统的研究,其构建的 BLdtugRPA24 菌株在以甘油为碳源的 pH-stat 流加发酵中积 累 5.2 g/L 胸苷[2,13,15-17]。因此,可以通过代谢 工程方法 定向改造 大肠杆菌 使其大量 积 累 胸苷。
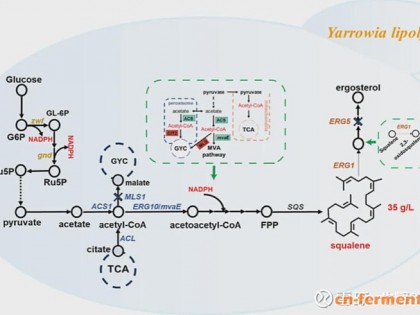
本文首先敲除了 E. coli BL21 (DE3) 补救 途径的 deoA 、tdk 、udp 三个基因,截断其分解 途径;随后敲除了 pgi 基因和 pyrL 序列,增加 胸苷前体物的供应,并通过过表达大肠杆菌胸 苷合成途径的 ushA 、thyA 、dut 、ndk 、nrdA 、 nrdB 六个基因来增加胸苷的合成通量 (图 1)。 最后,初步考查了各工程菌生产胸苷的能力, 其中 最终菌 株 BS08 在 摇瓶发酵 中积累 272 mg/L 胸苷,在分批补料发酵中可积累胸苷 1 248.8 mg/L 。


图 1 胸苷合成途径[13]
Fig. 1 Thymidine biosynthetic pathway. Genes and their corresponding enzymes were shown as follows: carAB , carbamoylphosphate synthetase; pyrBI , aspartate carbamoyl transferase; pyrC , dihydroorotase; pyrD , dihydroorotate oxidase; pyrE , orotate phosphoribosyltransferase; pyrF , OMP decarboxylase; pyrG , CTP synthetase; pyrH , nucleoside phosphate kinase; nrd , nucleotide diphosphate reductase; ndk , nucleoside diphosphate kinase; dut , deoxyribonucleotide triphosphatase; thyA , thymidylate synthase; ushA , 5’-deoxyribonucleotidase; deoA , thymidine phosphorylase; tdk , thymidine kinase; udp , uridine phosphorylase. The overexpressed genes in this study are indicated by the bold arrows. This figure is consulted with the figure of Lee et al [13].
1 材料与方法
1.1 菌株和质粒
菌株与质粒见表 1。Escherichia. coli BL21 (D E 3) 作为基因 敲 除和质粒表 达的宿主菌 , E. coli DH5α 作为质粒构建的宿主菌。
1.2 试剂与仪器
酵母抽提物、胰蛋白胨、基因组提取试剂 盒、DNA 胶回收试剂盒、PCR 产物纯化试剂盒 等均购自上海生工生物工程有限公司。快速高 保真 DNA 聚合酶 Fast pfu 购自北京全式金生物 技术有限公司。限制性内切酶和 T4 DNA 连接 酶均购自加拿大富酶泰斯 Fermentas 公司。其他 试剂为国产分析纯。
仪器:TU1901 双光束紫外可见分光光度计 (北京普析通用仪器有限公司);BLBIO-5GJ 发酵罐 (上海百仑生物科技有限公司);SBA40E 生物传感 仪 (山东省科学院生物研究所);HP 1100 LC 高效
液相色谱仪 (Agilent 188 Technologies, USA)。
1.3 发酵培养
种子培养基:10 g/L 胰蛋白胨,5 g/L 酵母 抽提物,5 g/L 氯化钠; 摇瓶发酵培养基:10 g/L 胰蛋白胨,5 g/L 酵母抽提物,5 g/L 氯化钠, 0.1 mol/L 3-吗啉丙磺酸 (MOPS),10 g/L 葡萄糖; 流加发酵初始培养基:15 g/L 胰蛋白胨,10 g/L 酵 母抽提物,5 g /L 氯化钠,0.4 g/L MgSO 4·7H 2O, 20 g/L 葡萄糖;流加培养基:454.5 g/L 葡萄糖与 22.7 g/L 酵母抽提物混合液。上述培养基在需要时添加 50 μg/mL 氨苄青霉素和 20 μg/mL 四环素。 摇瓶培养:取–80 ℃保藏的种子培养液接入 50 mL LB 种子培养基中,37 ℃、220 r/min 培养。 待 OD 长到对数中后期,以 OD 600 为 0.05 的初始 接种量接入到 100 mL 的发酵培养基中,37 ℃、 220 r/min 条件下培养。OD 600 达到 0.4 时,添加终 浓度为 0.5 mmol/L IPTG 诱导质粒上基因的表达。

表 1 菌株与质粒
发酵罐培养:种子液生长至对数中期时, 以 5%的接种量接种到含有 2.5 L 发酵液的 5 L 发酵罐中,在 37 ℃条件下进行培养。OD 600 达 到 0.6–0.8 之 间时, 添加 IPTG 至终 浓度为 0.5 mmol/L 。通过溶氧和转速的偶联控制使溶氧 水平保持在 20%–30%之间, 通气量为 1 vvm 。 通过添加 10% NH 4OH 调节发酵液 pH 维持在 7.0。当葡萄糖浓度低于 5 g/L 时,添加 110 mL 流加培养基。发酵结束时,补料添加的葡萄糖 大约为 250 g ,最终体积在 2.9–3.0 L 之间。
1.4 基因敲除
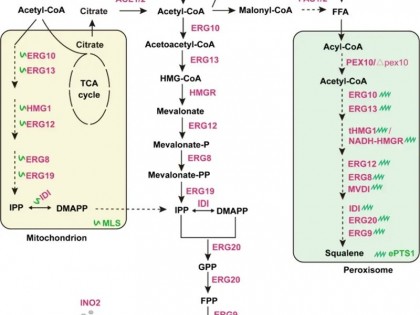
如图 2 所示,本实验先用 PCR 扩增出待敲除基
因的上游 F 和下游 D 各 片 段,通过融 合 PCR 扩 增出片 段 F-tet-D
[19]
。将片段 F-tet-D 电转入含有 pTKRED 质
粒的感受态细胞中,利用 red 重组系统进行同源重 组,筛选出 tetA 片段取代了待敲除基因的菌株[20]。 其后诱导Ⅰ-Sce Ⅰ酶表达,在 F-tet-D 片段内的 Ⅰ-Sce Ⅰ酶切位点进行酶切,导致该位点发生 DNA 双链断裂。断裂的基因组通过设计的 30 bp 同源片段进行同源重组,通过菌落 PCR 验证筛选 出目的基因敲除菌株[21]。敲除成功的菌落通过在 42 ℃下试管培养,可以消除胞内的 pTKRED 质粒。

图 2 基因敲除
Fig. 2 Gene disruption.
1.5 质粒的构建
首先提取 Escherichia coli BL21 (DE3) 基因 组 DNA 并以其为模板,按照引物 ushA-F/ushA-B 进行 ushA 基因的 PCR 扩增。纯化后的 ushA 基 因片段与载体 p5C 分别经 Sac Ⅰ和 Sma Ⅰ双酶 切,酶切产物纯化后用 T4 DNA 连接酶连接得 到表达载体 pLS1,并电转化到感受态细胞,涂 布含有氨苄青霉素的 LB 平板,挑选抗性克隆, 提质粒进行 Sac Ⅰ和 Sma Ⅰ双酶切鉴定,对鉴定 正确的质粒送测序验证。用同样方法,在 pLS1 质粒上依次插入了基因 thyA 、dut 和 ndk ,得到 质粒 pLS4。pLS4 质粒上的 ushA 、thyA 、dut 和 ndk 四个基因的转录由强启动子 P trc 控制。采用 同样的方法在 pTRC99A 上克隆了 nrdA 和 nrdB 基因,得到 pLM2 质粒。pLM2 上编码核苷二磷 酸还原酶的 nrdA 和 nrdB 基因的转录也被强启 动子 P trc 控制。 引物见表 2。
1.6 数据测定
1) 菌体密度:取发酵液经适当稀释,在 600 nm 下测定吸光度,本文中所有数据结果均为 3 组 平行实验的平均值。2) 发酵液中的残余葡萄糖: 发 酵 液离心 取 上清, 稀 释到适 当 倍数, 用
SBA40E 生物传感仪测定残余葡萄糖。3) 胸苷 的测定:发酵液离心取上清,膜过滤后用高效 液相色谱直接测定发酵液内胸苷的浓度。色谱 条件为:luna C18(2) (5 µm ,150 mm×4.6 mm) 为分离柱, V ( 乙腈 ) : V ( 三氟乙酸 ) : V (水)=4∶0.05∶95.5 为流动相,流速为 1 mL/min , 测定波长为 260 nm
[13]。4) 胞内 CTP 和 dUTP
用高氯酸法抽提 [22] ,色谱条件为: Agilent ZORBAX SB-Aq (5 μm ,250 mm×4.6 mm)为分 离柱,0.2 mol/L 磷酸盐缓冲液 (含有 10 mmol/L 的四丁基溴化铵):乙腈=89.5∶10.5 为流动相, 流速为 1 mL/min ,测定波长为 254 nm [23]。
表 2 过表达基因引物

2 结果与分析
2.1 基因敲除菌株的构建
F-tet-D 通过双交换同源重组整合到基因组 上,PCR 产物如图 3A 所示。tetA 经过分子内同 源重组被成功剔除出基因组,其相应的 PCR 产 物如图 3B 所示,并将 PCR 产物进行测序验证 基因敲除成功。验证结果正确的菌落在 42 ℃培 养以消除 pTKRED 质粒,得到菌株 BS01。同样 的方法依次敲除了 tdk 、udp 、pgi 和 pyrL 基因。
2.2 胸苷磷酸化酶 (deoA )、胸苷激酶 (tdk ) 和 尿苷磷酸化酶 (udp ) 基因敲除对菌株生产胸 苷的影响
补救途径合成嘧啶核苷酸需要胸苷磷酸化 酶、胸苷激酶、尿苷磷酸化酶,而这 3 个酶也催 化胸苷分解为胸腺嘧啶和生成 dTMP 。在野生型
菌株的基础上,敲除基因 deoA 、tdk 和 udp ,得 到 BS01 (Δde oA ) 、 BS02 (ΔdeoA Δtdk ) 和 BS03 (ΔdeoA Δtdk Δudp )。对这 3 株菌进行摇瓶发酵,通 过高效液相色谱法对发酵液进行检测。BS01 和 BS02 在整个发酵过程中未检测到胸苷的生成, 这说明胸苷的分解途径还没有完全被阻断 。 BS03 在发酵过程中的最大比生长速率为 1.44 h –1, 9 h OD 600 达到 7.86,发酵 9 h 消耗了 10 g/L 的 葡萄糖,积累了 22.8 mg/L 的胸苷。发酵 24 h 时胸苷浓度为 21.6 mg/L ,仅有微量下降,如图 4 所示。发酵结果表明,在同时敲除这 3 个基因 的情况下才能有效截断胸苷分解途径,使细胞 积累少量的胸苷。这和 Lee 等[13]的研究结果一 致,他们构建的遗传背景类似的菌株 BLdtu 也 消除了胸苷的降解,在以甘油为碳源的丰富培 养基中可以积累 12 mg/L 的胸苷。

图 3 菌落 PCR 验证
Fig. 3 colony PCR verification. (A) The fragments amplified by F1/T2 and T1/B3 were 1 350 bp and 1 201 bp. The T1 and T2 were internal primers of tetA . (B) The fragment after tetA disrupted was about 650 bp.

图 4 BS03 发酵曲线
Fig. 4 Fermentation using strain BS03.
2.3 pgi 和 pyrL 基因敲除对生产胸苷的影响
为了增加胸苷前体物的供给,敲除了 pgi 基 因,构建了 BS04 菌株。BS04 发酵结果如图 5 所 示,对数期的比生长速率为 0.53 h –1
,发酵 24 h 进入稳定期,葡萄糖被耗尽。与菌株 BS03 相比, 菌株 BS04 的比生长速率下降了 63%,发酵时间 增长,但最终菌体密度较高 (44 h 的 OD 600=15.2)。 最终胸苷的浓度为 78.7 mg/L ,相对于菌株 BS03 的产量提高了 3.6 倍。
在嘧啶核苷酸从头合成途径中,核苷二磷

图 5 BS04 和 BS05 发酵曲线
Fig. 5 Fermentation using strains BS04 and BS05.
酸还原酶和二氢叶酸还原酶都需要 NADPH 为 辅因子,核糖-5-磷酸是嘧啶核苷酸和嘌呤核苷 酸的共同前体,而核糖-5-磷酸和 NADPH 都是 在磷酸戊糖途径合成的。pgi 基因是 EMP 途径 的必需基因,敲除 pgi 能够阻止葡萄糖-6-磷酸 异构为果糖-6-磷酸,使葡萄糖-6-磷酸流向磷酸 戊糖途径,增加磷酸戊糖途径的通量,为胸苷的 合成提供更多的前体物。Hyeon Cheol Lee 等[16] 在 BLdtug24 的基础上敲除了 pgi 基因,构建出 BLdtugp24 菌 株。采用 pH-stat 流 加方式 , BLdtugp24 胸苷产量达到 1.02 g/L ,比出发菌株 BLdtug24 的产量提高了 4.86 倍。
天冬氨酸氨甲酰基转移酶是嘧啶核苷酸从 头合成途径的第一个关键酶,pyrB 和 pyrI 分别 编码其催化亚基和调节亚基,构成一个操纵子。 pyrB 上游有一段调控序列 pyrL ,其序列内部包 含有一个不依赖于ρ因子的转录终止子。研究表 明,在胞内 UTP 浓度较高时,大约 98%的转录 均在此位点终止[24]。敲除 pyrL 调控序列可以解 除 UTP 对 pyrBI 操纵子转录的弱化作用[25]。为 了 pyrBI 可以组成型表达,在 BS04 基础上敲除 了 pyrL 调控序列,构建了 BS05 菌株。如图 5 所示,该菌株对数期的比生长速率与 BS04 一 致,发酵 24 h 时进入稳定期,pyrL 敲除对菌体 生长速率几乎没有影响。发酵产物检测最终胸 苷的产量达到 90.5 mg/L ,与 BS04 相比,菌株 BS05 胸苷产量提高了 15%。
2.4 过表达 ushA 、th yA 、dut 、ndk 、nrdA 和 nrdB 对胸苷生产的影响
为了进一步提高胸苷的产量,过表达 UDP
到胸苷的核苷二磷酸还原酶 (nrdAB )、核苷二磷 酸激酶 (ndk )、dUTP 酶 (dut )、胸苷酸合酶 (thyA ) 和脱氧核糖核苷酸酶 (ushA )。首先在 BS05 菌株 中导入 pLS4 质粒,得到 BS06 菌株。同样在 BS05 菌株中导入 pLM2 质粒,得到 BS07 菌株。将 pLS4 和 pLM2 同时转入 BS05 中,得到重组菌 株 BS08。
为了考察 BS06、BS07 和 BS08 生产胸苷的 能力,对这 3 株菌分别进行了发酵。发酵结果见 表 3,BS06 发酵 44 h 时积累 100.7 mg/L 的胸苷,比 BS05 提高了 11.3%,其得率为 10.3 mg/(g glucose)。 而 BS07 菌株发酵 64 h 可以积累 169.2 mg/L 的胸苷,是 BS05 菌株的 1.87 倍,其得率为 18.6 mg/(g glucose)。BS07 对数期的比生长速率 0.46 h –1
,发酵 52 h 进入稳定期,生长迟滞期变长。 同时过表达 6 个基因的 BS08 菌株,64 h 可以积 累 272 mg/L 的胸苷,是 BS06 产量的 2.7 倍,BS07 产量的 1.6 倍,其得率达到 23.3 mg/(g glucose)。 由表 3 可以看出,BS06 胞内 dUTP/CTP 与 BS05 基本一致,BS07 胞内 dUTP/CTP 较 BS05 有微 量增加,而 BS08 胞内 dUTP/CTP 显著增加,这 表明过表达这 6 个基因增加了 UDP 到胸苷的通 量,使更多的 UDP 流向胸苷而不是 CTP 。
鉴于 BS08 是这些工程菌中产量最高的菌株, 对 BS08 进行了初步的补料发酵实验。如图 6 所 示,BS08 在 64 h 时达到最大 OD 600 约为 47.5。当
发酵 80 h 时,胸苷的产量达到 1 248.8 mg/L ,是摇 瓶发酵的 4.6 倍,生产率达到 15.61 mg/(L·h),得率 为 12.5 mg/(g glucose)。Lee 等
[16]
构建的菌株
BLdtugp24,敲除了 deoA 、tdk 、udp 、ung (编码 尿嘧啶-DNA 糖基化酶,对错配 DNA 进行碱基 切除修复) 和 pgi 基因,过表达了来自 PBS2 噬 菌体的 TMPase ,来自 T4 噬菌体的胸苷酸合酶、 核苷二磷酸 还原酶 ( n r d A B ) 和硫 氧还蛋 白 (nrdC ),以及大肠杆菌自身的尿苷激酶与 dCTP 脱氨酶 (udk -dcd 操纵子)。本研究在菌株改造的 代谢策略与 Lee 等[13]的研究有所不同:考虑到 敲除 ung 基因会影响细胞的遗传稳定性,本研 究并没有敲除 ung ;另一方面,由于 E. coli 中嘧 啶核苷酸从头合成途径的第一个关键酶天冬氨 酸氨甲酰基转移酶的转录表达受到严格的弱化 调控,因此,敲除了 pyrL 序列使其编码基因 p y rB I 可以组成型表达。在葡萄糖为碳 源的 pH-stat 流加发酵中,BLdtugp24 在 64 h 可以积累 1.02 g/L 胸苷,生产率为 15.8 mg/(L·h),得率为 6.1 mg/(g glucose)[16]。在分批补料发酵过程中, BS08 的胸苷 产量比 BLdtugp24 产 量要高 约 22% ,但值得注意的 是其最大细 胞干重只 有 BLdtugp24 的 42.6%,这表明在流加发酵工艺方 面,仍需要进一步优化来提高生物量和胸苷产 量。天冬氨酸也是胸苷的前体物之一,并且其 价格低廉,因此也可以尝试直接向培养基中添 加适量天冬氨酸来增加胸苷的合成通量。从分 批补料发酵结果中可以看出,菌体生长延迟期较 长,可以通过优化 IPTG 加入时间来有效缩短延 迟期,提高合成胸苷的生产率。或者尝试改用 pH-stat 流加发酵方式来代替分批补料发酵,可能 会取得更好的效果。另外,Koo 等还构建了工程 菌 BL dt u g R P A 24 ,该 菌株并 没有 敲除 pgi ,


表 3 基因过表达对胸苷生产的影响
metabolites were obtained at mid-log phase. 1.0 OD 600 = 0.45 g DCW/L.
大肠杆菌胸苷合成途径的 ushA 、thyA 、dut 、ndk 、 nrdA 和 nrdB 六个基因来增加胸苷的合成通量,BS08 菌株在摇瓶条件下可以积累 272 mg/L 胸苷,在分 批补料发酵条件下,胸苷的产量达到 1 248.8 mg/L , 生产率为 15.61 mg/(L·h),得率为 12.5 mg/(g glucose)。
REFERENCES
图6 BS08分批补料发酵
Fig . 6 Fed-batch fermentation using strain BS08.
而是敲除 purR 、pepA 和 argR 三个基因以提高
carAB 操纵子的转录水平。该菌株更适合利用甘油 为底物生产胸苷,在 pH-stat 流加发酵条件下积累 了 5.2 g/L 胸苷[2]。因此在代谢工程改造方面,BS08 的胸苷合成通量仍有很大的改进空间,这些问题 将在后续的工作中进一步研究与完善。
3 结论
本实验以 E. coli BL21 为出发菌株,敲除了嘧 啶核苷酸回补途径的 deoA 、tdk 和 udp 3 个基因, 使 BS03 能够积累 21.6 mg/L 胸苷。在 BS03 基础 上敲除了 pgi ,增加合成胸苷的前体物来源,BS04 可以积累 78.7 mg/L 胸苷,进一步敲除了 pyrL 序 列,使 pyrBI 组成型表达,BS05 胸苷的产量达到 90.5 mg/L ,较 BS03 提高了 4.2 倍。随后过表达了
[1] Cooper DL, Lovett ST. Toxicity and tolerance
mechanisms for azidothymidine, a replication gap-promoti ng agent, in Escherichia coli. DNA Repair, 2011, 10(3): 260–270.
[2] Koo BS, Hyun HH, Kim SY , et al . Enhancement
of thymidine production in E. coli by eliminating repressors regulating the carbamoyl phosphate synthetase operon. Biotechnol Lett, 2011, 33(1): 71–78.
[3] Song KH, Kwon DY , Kim SY , et al. Thymidine
production by Corynebacterium ammoniagenes mutants. J Micro Biol Biotechnol, 2005, 15(3): 477–483.
[4] Tsen S. Chemostat selection of Escherichia coli
mutants secreting thymidine, cytosine, uracil, guanine, and thymine. Appl Microbiol Biotechnol, 1994, 41(2): 233–238.
[5] Xu Y. Study on the technology of enzymatic
synthesis of thymidine and cytidi ne[D]. Hangzhou: Zhejiang University of Technology, 2009 (in Chinese).
徐渊. 酶法生物合成胸苷和胞苷工艺的研究[D]. 杭州: 浙江工业大学, 2009.
[6] Chang GQ, Ou L, Ding QB, et al. Breeding of thymineless Escherichia Coli mutated with N + ions implantation. Chem Bioeng, 2011, 28(4): 49–52 (in Chinese).
昌国强, 欧伶, 丁庆豹, 等. N +离子注入诱变筛 选胸腺嘧啶缺陷型大肠杆菌. 化学与生物工程, 2011, 28(4): 49–52.
[7] Shen RK, Qiu WR, Sun NX. Enzymatic synthesi s
of thymidine by nucleoside phosphorylases in Escherihia coli . J East China Univer Sci Technol, 1996, 22(6): 701–705 (in Chinese).
沈荣坤, 邱蔚然, 孙南翔. 应用大肠杆菌的核苷 磷酸化酶合 成胸苷 . 华东 理工大学学 报 , 1996, 22(6): 701–705.
[8] Qiu WR, Shen RK. Enzymatic synthesis of
thymidine. Chin Pharmac, 1995, 26(9): 424–427. 邱蔚然, 沈荣坤. 酶法合成胸苷. 中国医药工业 杂志, 1995, 26(9): 424–427 (in Chinese).
[9] Pierard A, Glansdorff N, Gigot D, et al. Repression
of Escherichia coli carbamoylphosphate synthase: relationships with enzyme synthesi s in the argi nine and pyrimidine pathways. J Bacteriol, 1976, 127(1): 291–301.
[10] Kantrowitz ER. Allostery and cooperativity in
Escherichia coli aspartate transcarbamoylase. Archives Biochem Biophys, 2012, 519(2): 81–90. [11] Turnbough CL. Regulation of gene expression by
reiterative transcription. Curr Opin Microbiol, 2011, 14(2): 142–147.
[12] Wilson HR, Turnbough CL. Role of the purine
repressor in the regulation of pyrimidine gene expression in Escherichia coli K-12. J Bacteriol, 1990, 172(6): 3208–3213.
[13] Lee HC, Kim JH, Kim JS, et al . Fermentative
production of thymidine by a metabolically engineered Escherichia coli strain. Appl Environ Microbiol, 2009a, 75(8): 2423–2432.
[14] Gaithersburg MR, Rockville AD. Fermentation
process for the producti on of pyrimidine deoxyribonucleosides: EP, 0504279B1. 1990-05–12. [15] Lee HC, Ahn JM, Lee SN, et al. Overproduction
of thymidine by recombinant Brevibacterium helvolum amplified with thymidine
monophosphate phosphohydrolase gene from bacteriophage PBS2 . Biotechnol Lett, 2004, 26(4): 265–268.
[16] Lee HC, Kim JS, Jang W, et al. High NADPH/NADP +
ratio improves thymidine production by a metabolically engineered Escherichia coli strai n. J Biotechnol, 2010, 149(1/2): 24–32 .
[17] Lee HC, Kim JS, Jang W, et al. Thymidine
production by overexpression NAD + kinase in an Escherichia coli recombinant strain. Biotechnol Lett, 2009, 31(12): 1929–1936.
[18] Kuhlman TE, Cox EC. Site-specific chromosomal
integration of large synthetic constructs. Nucleic Acids Res, 2010, 38(6): 92.
[19] Lin Z, Xu Z, Li Y, et al. metabolic engineering of
Escherichia coli for the production of riboflavin. Microb Cell Fact, 2014, 13: 104.
[20] Datsenko KA, Wanner BL. One-step inactivation
of chromosomal genes in Escherichia coli K-12 using PCR products. Proc Natl Acad Sci USA, 2000, 97(12): 6640–6645.
[21] Metcalf WW, Jian GH, Daniels LL. Conditionally
replicative and conjugative plasmids carrying lacZa for cloning, mutagenesis, and allel e replacement in bacteria. Plasmid, 1996, 35(1): 1–13. [22] Barrette WC, Albrich JM, Hurst JK. Hypochlorous
acid-promoted loss of metabolic energy in Escherichia coli. Infect Immun, 1987, 55(10): 2518–2525. [23] Müller RH, Loffhagen N, Babel W. Rapid
extraction of (di)nucleotides from bacterial cells and determination by ion-pair reversed-phase HPLC. J Microbiol Methods, 1996, 25(1): 29–35. [24] Turnbough CL, Hicks KL, Donahue JP.
Attenuation control of pyrBI operon expression in Escherichia coli K-12. Proc Natl Acad Sci USA, 1983, 80(2): 368–372.
[25] Levin HL, Schachman HK. Regulation of
aspartate transcarbamoylase synthesis in Escherichia coli : analysis of deletion mutations in the promoter region of the pyrBI operon. Proc Natl Acad Sci USA, 1985, 82(14): 4643–4647.