(集美大学 食品与生物工程学院,福建 厦门,361021)
摘 要 在5 L发酵罐中对α-L-鼠李糖苷酶进行小试发酵,制备酶液;以聚乙烯醇-海藻酸钠为包埋载体,以戊二醛为交联剂对该酶进行固定化。经5 L罐高密度发酵96 h,α-L-鼠李糖苷酶酶活为2 766 U/g,生物量为228 g/L。经过固定化后,α-L-鼠李糖苷酶的酶活为20 U/g,酶活回收率为32.88%,固定化α-L-鼠李糖苷酶的最适反应温度为35~50 ℃,最适反应pH值为4.0,该固定化酶在连续使用6次后酶活仍然保留98.22%。高密度发酵能显著提高酶的产量,同时固定化技术提高了酶的重复利用率,为该酶利用芦丁酶法转化制备异槲皮苷提供了依据。
关键词 α-L-鼠李糖苷酶;高密度发酵;酶固定化;异槲皮苷
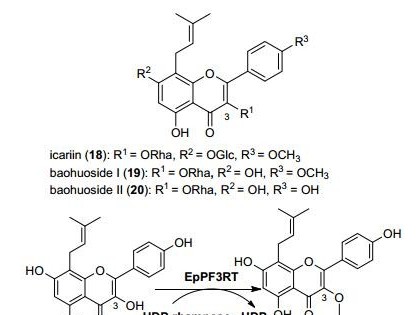
异槲皮苷是一种含有多个酚羟基的黄酮醇苷类化合物,具有消除炎症[1]、抗氧化活性[2]、降血糖[3]、降血压[4]、抗过敏[5]等药理作用。异槲皮苷的天然含量很少,往往通过水解芦丁来制备。常用的方法有强酸水解芦丁、有机溶剂提取、高压水解芦丁和酶水解芦丁等[6-8]。其中强酸和有机溶剂提取法对环境的污染严重,高压水解法对生产设备耐高温高压要求高、耗能较大,而利用酶水解芦丁操作工艺相对简单,反应条件温和且污染较少,具有重要研究应用价值。
α-L-鼠李糖苷酶(EC3.2.1.40)可用于制备异槲皮苷,通过水解芦丁上的1,6-α-鼠李糖苷键,生成异槲皮苷。吴迪[9]等人研究表明,运用芦丁-L-鼠李糖苷酶转化芦丁生产异槲皮苷,生产反应的条件温和、易于控制,是制备异槲皮苷的理想方法,因此研究相关酶的发酵生产具有重要意义。张雪铭[10]等人研究了黑曲霉α-L-鼠李糖苷酶高密度发酵条件,取得了一定成果。但黑曲霉发酵后需要通过纯化去除自身产生的其他多种蛋白,同时黑曲霉常见的固态发酵会产生菌丝体,为纯化带来不便[11]。毕赤酵母表达系统具有表达效率高,自身分泌蛋白少[12-13],胞外表达的目的蛋白易于纯化等特点[14];此外,毕赤酵母成熟的发酵工艺适用于高密度发酵,可满足α-L-鼠李糖苷酶的工业实际应用。研究发酵过程中甲醇的添加量是保证毕赤酵母不受甲醇毒害作用,保持正常分泌外源蛋白的重要因素[15]。α-L-鼠李糖苷酶的固定化能简化酶在反应体系中的分离工艺,提高酶的稳定性和重复利用率,节约成本同时简化催化工艺,提高生产效率[16]。因此,本研究通过优化甲醇的添加量提高了α-L-鼠李糖苷酶高密度发酵产量,并对该酶的固定化特性进行了研究,为工业化生产α-L-鼠李糖苷酶和酶法转化芦丁生产异槲皮苷提供依据。
1. 1 材料与试剂
重组毕赤酵母GS115/pPIC9k-rha菌株,由集美大学食品与生物工程学院发酵工程实验室保藏。芦丁(≥98%)购于西安小草植物科技有限责任公司;甲醇(GR)、乙腈(GR)购于美国西格玛奥德里奇有限公司;其他试剂均为分析纯。
1. 2 仪器与设备
BLBIO-5SJ 发酵罐,上海百仑生物科技有限公司;DGU/SPD/SIL-20A高效液相色谱仪,日本岛津仪器制造有限公司;ALP全自动灭菌锅,上海博迅医疗生物仪器股份有限公司;ZD-9550脱色摇床,海门其林贝尔仪器有限公司。
1. 3 实验方法
1.3.1 α-L-鼠李糖苷酶5 L发酵罐发酵培养
以3.325 g无氨基酵母氮源、3.725 mL甘油、0.1 mg生物素和250 mL无菌水配置成种子培养基接入1 mL重组毕赤酵母GS115/pPIC9k-rha菌株,于30 ℃、200 r/min的摇床中培养至有白色结晶出现,然后以5%的接种量接种到2.5 L的发酵培养基中,以体积分数为25%的NH4OH调节pH至5.0~6.0,在30 ℃及溶解氧高于40%的条件下发酵培养。
待培养基中的甘油耗尽后,进行流加甘油培养,初始流加速率为10 mL/(L·h),经过10 h后,将流速提升到500 mL/(L·h),培养酵母直至所需密度。发酵过程中每隔8 h取1次样测湿重及酶活。
甘油流加培养至所需密度后,停止补加甘油,将溶解氧调节至60%左右维持30 min,随后将发酵温度调节至28 ℃,pH值调节至pH 5.0继续发酵并开始流加甲醇。甲醇的流加速度最初2 h为3 mL/(L·h),之后每隔1 h增加1 mL/(L·h)。当流速为6 mL/(L·h)后,维持3~4 h。之后以发酵液2.5 L体积分数的0.17%、0.5%、1%每隔1 h补加甲醇,每隔8 h取1次样测酶活。经过3 d甲醇诱导后,获得发酵酶液。
1.3.2 生物量和酶活的测量
取1 mL的发酵液于1.5 mL的离心管中, 8 000 r/min离心2 min,倒掉上清液,洗涤烘干后称量得到菌体的干重[17]。
酶活测量采用高效液相色谱(HPLC)法[18]:量取1.0 mL质量浓度为300 μg/mL的芦丁标准溶液加入到10 mL的离心管中,再加入980 μL柠檬酸-磷酸氢二钠缓冲液(pH 4.0),漩涡混匀,置于60 ℃ 水浴锅中保温10 min,迅速加入20 μL酶溶液,混匀,在60 ℃恒温水浴锅中反应15 min后立即放入沸水中灭活12 min,冷却后过0.22 μm滤膜,空白对照组以灭活的酶液代替原酶溶液,其余步骤同上。然后利用高效液相色谱仪检测芦丁含量并依此计算酶活。使用Symmetry C18反相柱,柱温为35 ℃,紫外检测波长为280 nm,进样体积20 μL,流速0.25 mL/min,走样时间60 min,流动相为A: 0.5%甲酸水溶液,B:乙腈,经优化得出的梯度洗脱条件如表1所示。
表1液相洗脱条件
Table1Liquidphaseelutionconditions

α-L-鼠李糖苷酶酶活力单位的定义(U):以每分钟消耗1 μmol芦丁所需要的酶液量定义为1个α-L-鼠李糖苷酶活力单位。
1. 4 固定化酶凝胶颗粒的制备
称取0.1 g海藻酸钠和2.4 g聚乙烯醇加入34 mL无菌水加热溶解,冷却后加入0.5 mL的戊二醛静置1 h,在交联后的溶液中滴加质量浓度为9.3 mg/mL的酶液6 mL,放在恒温振动器(22 ℃,150 r/min)振动,2 h后加入1.6 g硼酸和0.4 g CaCl2搅拌造粒,15 min后放入质量浓度为10%的Na2SO4中4 h,进行固定化,得到固定化酶凝胶颗粒储存在pH 4.0的醋酸缓冲液中于4 ℃保存。
1. 5 固定化α- L- 鼠李糖苷酶性质测定
1.5.1 固定化α-L-鼠李糖苷酶酶活测定
酶活力测定的反应体系:0.98 mL柠檬酸缓冲液(20 mmol/L,pH 4.0)与1 mL质量浓度为300 μg/mL芦丁底物混合,置于50 ℃条件下温育10 min后,加入1 g固定化酶液混匀,于50 ℃反应15 min后,立即取出固定化酶,将体系置于100 ℃沸水浴10 min,冷却至室温,过0.22 μm水膜后用液相色谱测定芦丁含量的变化。空白反应是将加入的酶液换为100 ℃沸水灭活的酶。
1.5.2 固定化α-L-鼠李糖苷酶最适温度测定
最适温度:按一定比例将固定化酶加入到pH值为4的柠檬酸盐缓冲液中混匀,分别在30、35、40、45、50、55、和60 ℃的酶反应体系下反应15 min,测定α-L-鼠李糖苷酶酶活力,以酶活力最高的为100%,空白组以100 ℃灭活的酶液进行同样条件的酶反应。
1.5.3 固定化α-L-鼠李糖苷酶最适pH测定
最适pH:按一定比例将固定化酶加入到不同pH(2.0~6.0)的50 mmol/L柠檬酸盐缓冲液中,在50 ℃测定α-L-鼠李糖苷酶酶活力,以酶活力最高的为100%,空白组以100 ℃灭活的酶液进行同样条件的酶反应。
1.5.4 固定化α-L-鼠李糖苷酶底物动力学
以不同质量浓度的(12.5、25.0、50.0、100.0、150.0和200.0 μg/mL)芦丁为底物,在最适pH和最适温度的条件下,测定α-L-鼠李糖苷酶酶活力,按照Lineweaver-Burk plots双倒数曲线作图法计算重组酶对柚皮苷的米氏常数(Km)。
1.5.5 固定化α-L-鼠李糖苷酶操作半衰期及稳定性
将固定化酶置于pH为4的柠檬酸盐缓冲液中50 ℃温浴,每隔1 h取适量固定化酶依酶活反应体系测定酶活,以初始酶活为100%,计算相对酶活。
取适量固定化颗粒,在最适pH和最适温度的条件下按照酶活反应体系连续进行6批次操作,以最高酶活力作为100%计算相对酶活。
2 结果与讨论 2. 1 α- L- 鼠李糖苷酶发酵结果
α-L-鼠李糖苷酶发酵结果如图1所示。在5 L发酵罐中,当罐内溶氧量上升时,控制甲醇加入,体积分数分别为0.17%、0.5%和1%时,重组毕赤酵母GS115/pPIC9k-rha的酶活和生物量都呈现出随诱导时间增加而增加的趋势,诱导发酵到最后的酶活分别为1 865.8、2 766.0和1 979.9 U/mL,生物量能达到209、228和194 g/L。甲醇在毕赤酵母发酵过程中既是细胞生长所需的碳源又是菌体的能源物质,添加量过少,则菌体没有足够的能源用于分泌外源蛋白,故而酶活有所降低;而甲醇添加量如果过高,又会产生毒害作用,抑制细胞的生长甚至引起细胞死亡,同样会影响酶活结果。所以发酵过程中最适甲醇添加量为发酵液总体积的0.5%。与摇瓶发酵最适条件相比,发酵罐发酵后的酶活是摇瓶的3.89倍[19]。

A-不同甲醇添加量对酶活力的影响;B-不同甲醇添加量对生物量的影响
图1 不同甲醇添加量下酶活与生物量结果
Fig.1 Enzyme activity and biomass results of different methanol additives
采用SDS-PAGE鉴定重组α-L-鼠李糖苷酶,得到结果如图2,泳道中可见一单一条带,分子质量约100 kDa,与原始黑曲霉α-L-鼠李糖苷酶大小相似。整体来看发酵上清中目的蛋白纯度高,杂蛋白含量较低,可直接对发酵上清液进行固定化操作。

图2 重组α-L-鼠李糖苷酶SDS-PAGE图
Fig.2 SDS-PAGE of recombinant α-L-rhamnosidase
2. 2 固定化酶的制备
采用海藻酸钠聚乙烯醇制备固定化酶凝胶颗粒时,聚乙烯醇有利于增强凝胶的耐久性和机械强度,海藻酸钠能形成黏稠均匀溶液,可以改善凝胶的表面性质,减少聚集的可能[20]。最终制成的成品如图3,固定化α-L-鼠李糖苷酶珠子大小均匀,弹性好,圆润光滑,具有一定的机械强度,酶活为20 U/g,酶活回收率为32.88%。

图3 制备的固定化α-L-鼠李糖苷酶
Fig.3 The picture of immobilized α-L-rhamnosidase
2. 3 固定化α- L- 鼠李糖苷酶酶学性质研究
2.3.1 固定化酶最适温度
在酶促反应体系温度30~60 ℃,pH 4.0的条件下测定酶活力,确定固定化α-L-鼠李糖苷酶的最适温度。由图4可知,固定化α-L-鼠李糖苷酶的酶活力随着温度上升呈现先增高后降低的趋势。固定化酶的最适温度为50 ℃。而由前期实验得知游离酶的最适温度为60 ℃。因为固定化载体聚乙烯醇和海藻酸钠熔点较低,在温度高于50 ℃后固定化酶的胶质开始融化[21],受此因素影响使得该方法制备的固定化酶的耐热性较差。但固定化的α-L-鼠李糖苷酶在35~50 ℃之间维持了较高的催化活性,与游离酶相差不大。

图4 温度对固定化α-L-鼠李糖苷酶活力的影响
Fig.4 Effect of different temperature on residual activity of immobilized α-L-rhamnosidase
2.3.2 固定化酶最适pH
在温度为50 ℃的条件下,酶促反应体系的pH分别为2、3、4、5、6时测定固定化α-L-鼠李糖苷酶酶活。在pH为2时海藻酸钠降解明显,不能形成凝胶颗粒,所以该固定化酶的起始测定pH值为3。固定化酶最适pH的结果如图5所示,固定化α-L-鼠李糖苷酶的最适pH范围在3.0~4.0,与游离酶的最适pH相同。随着pH的继续升高,酶活迅速降低,说明该固定化酶是在酸性环境中催化性能较好。

图5 不同pH对固定化α-L-鼠李糖苷酶活力的影响
Fig.5 Effect of different pH on residual activity of immobilized α-L-rhamnosidase
2.3.3 动力学参数的测定分析
在60 ℃下,在pH为4.0的条件下以不同浓度的芦丁作为底物,测定固定化α-L-鼠李糖苷酶的酶活并计算其反应初速率,以1/[S]为横坐标,1/[V]为纵坐标制作Lineweaver-Burk双倒数的拟合曲线,得到动力学结果如图6,Lineweaver-Burk双倒数的拟合方程为y=0.449 4x+0.000 16,R2=0.97。计算固定化酶酶解反应的米氏常数Km为0.47 mmol/L,而前期实验得知游离酶的Km为0.25 mmol/L,酶固定化后的Km值相较于游离酶变大。NUNES[22]等人研究固定柚苷酶的过程中,固定化酶的Km值也比游离酶大,这表明底物固定化以后由于树脂载体内部的空间位阻和扩散效应造成酶与底物的亲和性降低,反应初速率有一定增大。

图6 固定化α-L-鼠李糖苷酶的Lineweaver-Burk图
Fig.6 Lineweaver-Burk plot for immobilized α-L-rhamnosidase
2.3.4 半衰期及操作稳定性
重组α-L-鼠李糖苷酶的半衰期如图7所示,在6 h的时候,酶活下降为初始酶活的50%。随着操作次数的增多,反应体系中固定化α-L-鼠李糖苷酶的酶活变化情况如图7所示。

A-固定化α-L-鼠李糖苷酶的半衰期;B-固定化α-L-鼠李糖苷酶操作稳定性
图7 固定化α-L-鼠李糖苷酶的半衰期和操作稳定性
Fig.7 Half-life and operation stability of immobilized α-L-rhamnosidase
固定化α-L-鼠李糖苷酶的酶活随着反应次数的增多而逐步上升。出现这种情况的原因可能是初始阶段的聚乙烯醇-海藻酸钠载体强度较大但传质性能比较差,产生了一定的空间位组和屏蔽作用,从而对酶的活性产生影响[16]。而后随着反应次数的增加,载体强度减弱,被包埋的酶渐渐与底物接触,芦丁转化强度变大,连续使用了6次后凝胶颗粒基本上已经处于透明胶化的状态,但相对酶活还能保持在98.22%。说明该固定化α-L-鼠李糖苷酶有着比较好的操作稳定性,利于重复利用,具工业化大规模生产的潜能。
3 结论
本文对重组黑曲霉α-L-鼠李糖苷酶进行了5 L罐高密度发酵和酶固定化实验,并对固定化α-L-鼠李糖苷酶性质进行了测定。通过采取不同甲醇流加量发现当甲醇添加的体积分数为0.5%时,酶活力达到最高2 766 U/mL ;采用质量分数1%海藻酸钠和体积分数10%戊二醛交联制作固定化α-L-鼠李糖苷酶,其最适温度为40 ℃,最适pH为4.0,固定化α-L-鼠李糖苷酶的酶活为20 U/g,酶活回收率为32.88%。以高密度发酵α-L-鼠李糖苷酶并进行固定化,为今后发酵工艺的进一步放大及α-L-鼠李糖苷酶制备异槲皮苷的工业化生产提供了理论依据和指导。
High density fermentation of α- L- rhamnosidase and enzymeimmobilization
LIU Jia-nan,GONG Jian-ye,GAO Ting,LI Li-jun*,NI Hui
(College of Food and Biological Engineering, Jimei University, Xiamen 361021, China)
ABSTRACT α-L-rhamnosidase produced by high density fermentation was immobilized into matrix consisting of polyvinyl alcohol and sodium alginate with glutaraldehyde as crosslinker. In the 5 L bioreactor, the activity of immobilized enzyme achieved 2 766 U/g and its biomass reached 228 g /L after 96 h cultivation. The enzyme activity recovery of 32.88% was obtained and the activity of immobilized enzyme was 20 U/g. The optimal temperature was 35-50 ℃ and the optimal reaction pH at about 4.0 for immobilized enzyme. The residual enzyme activity could retain more than 98.22% after 6 batches of recycling use. These results suggested that the high density fermentation could effectively enhance enzyme production, and the immobilization technology could improve enzyme recycling rate, which would offer a basis for large-scale production of isoquercitrin.
Key words α-L-rhamnosidase; high density fermentation; immobilized enzyme; isoquercitrin
DOI:10.13995/j.cnki.11-1802/ts.016143
引用格式:刘嘉男,巩建业,高庭,等.α-L-鼠李糖苷酶高密度发酵及其固定化[J].食品与发酵工业,2018,44(7):44-48;54. LIU Jia-nan,GONG Jian-ye,GAO Ting,et al.High density fermentation of α-L-rhamnosidase and enzyme immobilization[J].Food and Fermentation Industries,2018,44(7):44-48;54.
第一作者:硕士研究生(李利君副教授为通讯作者,E-mail:ljli@jmu.edu.cn)。
基金项目:国家自然基金(31371751)
收稿日期:2017-10-29,改回日期:201-01-26