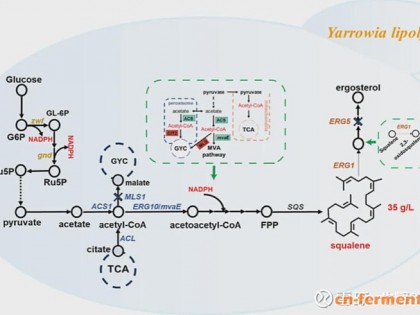
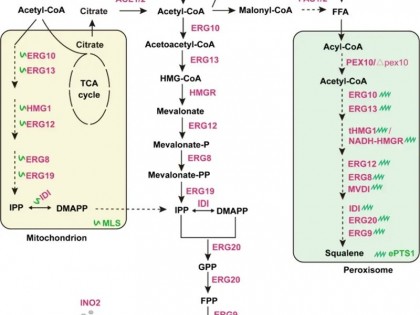
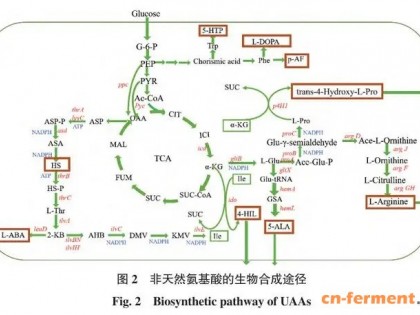
逆向合成分析是化学合成中广泛使用的有效方法,受到越来越多的关注。化学反向合成分析主要基于差异:目标产物的碳骨架通过碳碳键裂解和适当的官能团转化被切割成不同的小分子片段。前体的匹配通常不是问题。然而,生物合成途径通常始于单一碳源如葡萄糖。北京化工大学An-ping Zeng实验室的研究者提出了一种碳骨架重建(Carbon Skeleton Reconstruction,CSR)的反向生物合成方法,用于合成天然次级代谢产物5-氨基乙酰丙酸(5-aminolevulinic acid,5-ALA),相关研究结果发表在ACS Synthetic Biology杂志。
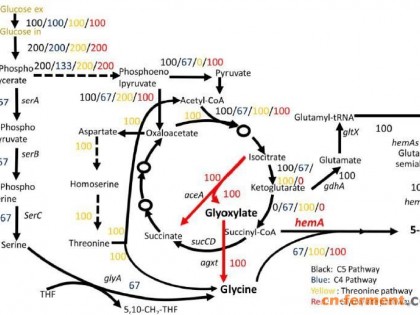
5-ALA是分别在第四和第五碳上具有酮基和氨基的五碳酸,它是叶绿素,血红素和维生素B12生物合成途径的中间体,在农业,医药和有机合成中具有重要作用。目前,5-ALA主要由糠醛,四氢糠胺或乙酰丙酸化学合成,起始材料有限或成本相对较高,需要多步功能组转换。此外,反应条件通常是苛刻、并且会使用有毒溶剂。微生物可通过两种不同的途径从葡萄糖合成5-ALA:即“C5途径”和“C4途径”(图1)。C4途径比C5途径更简单和可控,因此受到很多关注。C4途径的关键问题之一是甘氨酸的供应和与其它前体的匹配。甘氨酸的供应限制了5-ALA的产率和产率。

ε-氨基酮基的碳-碳键可以裂解成亲电子C4部分和亲核氨基甲基C1部分。在C4途径中,甘氨酸通过丝氨酸途径合成,导致碳原子浪费并造成C1代谢调节的问题。如果要将5-ALA扩大作为生物产品,那么最重要的问题是平衡两种前体甘氨酸和琥珀酸的通量。除丝氨酸途径外,甘氨酸还可以从苏氨酸裂解途径和乙醛酸途径中获得。但苏氨酸本身具有较长的合成途径,且合成通量不高,使其很难成为供应甘氨酸的主要途径。乙醛酸转氨酶可逆催化生成甘氨酸;异柠檬酸裂解合成乙醛酸和琥珀酸(琥珀酰CoA酯是合成5-ALA的中间体),因此使用乙醛酸分流和异源丙氨酸乙醛酸氨基转移酶,可以建立一条合成5-ALA的非天然途径。胞外和(大肠杆菌)胞内实验证明了这一途径的可行性。新的5-ALA途径对于避免甘氨酸供应问题非常有用,因为甘氨酸供应在文献中已被证明是难以设计的。